Методы лечения рака предстательной железы — степени заболевания, диагностика и терапия
Злокачественные опухоли клеток простаты приводят к серьезному заболеванию мужчин, лечение рака предстательной железы может проводиться разными методами – от операции до народных средств. Важно вовремя заметить признаки течения заболевания и наблюдаться у врача, чтобы минимизировать риск развития осложнений. На запущенных стадиях рака предстательной железы сложно добиться полного выздоровления, если в теле уже есть метастазы.
Что такое рак предстательной железы
Согласно медицинскому определению, рак простаты у мужчин – это онкологическое заболевание предстательной железы у мужчин. Она входит в органы репродуктивной системе, служит для частичного производства семенной жидкости, участвует в процессе семяизвержения и удерживания мочи. Наличие в предстательной железе злокачественных опухолей приводит к раку. Им страдают мужчины в возрасте после 55 лет.
Сегодня рак простаты занимает лидирующие места среди мужских онкологических заболеваний по всему миру. Особенность его протекания заключается в медленном развитии без заметных симптомов. Для исключения риска возникновения осложнений мужчинам после 45 лет регулярно рекомендуется проходить осмотр у андрологов и сдавать анализы. Раннее обнаружение рака предстательной железы даст больше шансов на выздоровление.
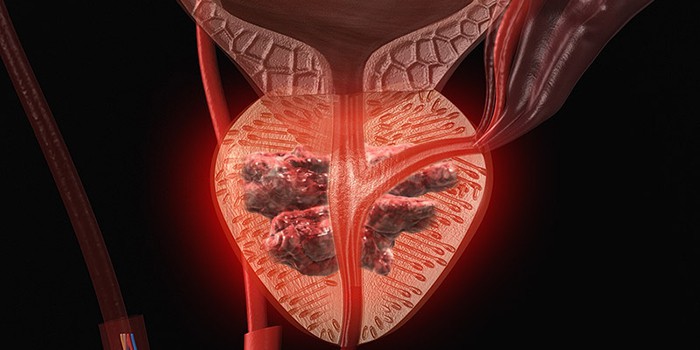
Лечится ли рак предстательной железы
Возможный диагноз опухоль простаты ставится на основании следующих симптоматических признаков:
- боли при опорожнении мочевого пузыря, затруднение процесса;
- половые расстройства, эректильная дисфункция.
Такие симптомы схожи у рака с доброкачественной опухолью (аденомой предстательной железы) и гиперплазией (увеличением простаты). Отличием злокачественного образования становится возможность нарушить эрекцию при затрагивании нервов и уменьшить объем спермы из-за блокировки эякуляторного канала. На поздних стадиях рака предстательной железы заметны кровь в моче, болезненные ощущения по всему телу. При образовании метастаз болит спина, ноги, развитие происходит в печени, надпочечниках, легких, костях.
Четвертая патологическая стадия рака требует длительного серьезного лечения, но даже тут врачи не уверены в благоприятном прогнозе. Факторами риска возникновения онкологии становятся:
- генетическая предрасположенность;
- плохая экология;
- проблема неправильного питания – большое количество принимаемых мяса, молока, яиц;
- прогрессирующая аденома.
Для профилактики возникновения заболевания рака предстательной железы врачи рекомендуют соблюдать простые правила:
- вести здоровый образ жизни, отказаться от алкоголя, курения;
- заниматься спортом;
- включить в рацион больше томатов, капусты, брокколи, сои, винограда;
- ограничить прием продуктов на основе животных жиров и с большим количеством кальция.
Лечение рака простаты
Любая процедура лечения начинается с диагностики, на основании которой выносится решение о принимаемом методе терапии рака предстательной железы:
- пальцевое ректальное исследование – для прощупывания тканей простаты на предмет опухолей;
- трансректальное УЗИ .
- анализ крови на специфические антигены;
- биопсия и гистологическое исследование клеток;
- компьютерная томография;
- остеосцинтиграфия – для определения степени распространения рака.
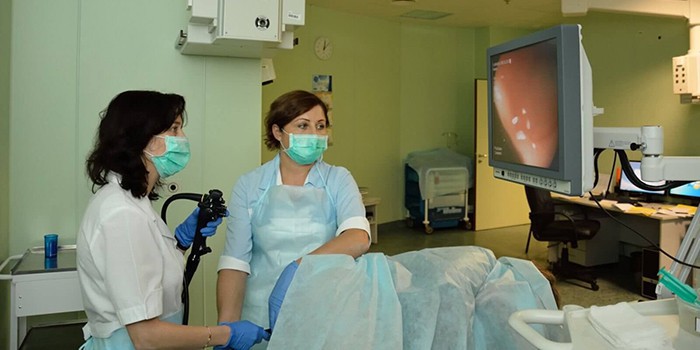
Методы лечения
От стадии развития рака предстательной железы зависят дальнейшие методы лечения. Основными способами считаются:
- хирургический, включающий трансуретральную резекцию простаты;
- лучевая терапия – радиотерапия;
- гормональная терапия;
- химиотерапия.
Медикаментами
Лечение рака без операции проводится медикаментозными средствами. При терапии предстательной железы применяются патогенетические лекарства, способствующие восстановлению нарушенных функций, улучшению метаболизма, укреплению иммунитета. Вот популярные группы препаратов:
- Аспирин – ингибирует синтез простагландинов – гормоноподобных веществ;
- Верошпирон – подавляет выработку некоторых гормонов;
- экстракты женьшеня, эхинацеи, Бефунгин, стимулятор Дорогова, АСД – адаптогены;
- Талидомид – модулирует иммунную систему;
- Циклоферон, Реаферон, Виферон – воздействуют на интерфероновую систему;
- для облегчения мочеиспускания – Омник;
- антибактериальные средства – Вибрамицин, Юнидокс Солютаб;
- анальгетики – Парацетамол, Диклофенак, Трамадол;
- поддерживающие печень средства – Лейкомакс, Эпиталамин;
- для снятия нейропатической боли – Лирика;
- гомеопатия – Гепар сульфур.




В медикаментозной терапии рака предстательной железы пожилых используют несколько другие препараты, которые сокращают выработку тестостерона и андрогена:
- Люпрон;
- Бусерелин-депо;
- Элигард;
- Золадекс;
- Эулексин;
- Касодекс;
- Ниландрон;
- Эстрацит – инъекции;
- Паклитаксел;
- Новантрон;
- Проскар;
- Альфарадин;
- Пролиа.
Орхиэктомия
Хирургическим способом лечения является орхиэктомия при раке предстательной железы, представляющая собой удаление яичек, ответственных за выработку тестостерона, из области таза. Процедура применяется для больных с метастазами, имеет быстрый эффект. К преимуществам операции на предстательной железе относятся эффективный клинический результат, моментальное снижение выработки тестостерона без повышения уровня пролактина в крови.
Выделяют следующие разновидности хирургического вмешательства в предстательную железу, отличающиеся результатом и сложностью:
- билатеральная тотальная – полное удаление органа, не всегда позволяет снизить тестостерон до кастрационных величин;
- радикальная простатэктомия – локализованное удаление простаты, менее травматичным методом является эндоскопическое вмешательство, после него пациенту гарантируют 10-15 лет жизни;
- субкапсулярная эпидидиморхиэктомия – при ней не удаляются белочная оболочка и придаток, процедура более приемлема по косметическим соображениям.
Радиотерапия
Лечение рака предстательной железы может производиться радиотерапией – дистанционным лучевым воздействием. Оно выполняется на линейных ускорителях при помощи компьютера. Индивидуальный подход к лечению рака сводит к минимуму все побочные явления. После облучения пациенту выписываются лекарства, производится гормонотерапия. Для увеличения продолжительности жизни прописывается диета.
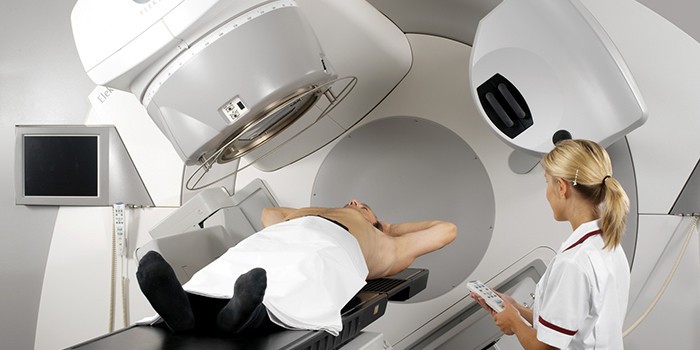
Криотерапия
Использование экстремально холодных температур применяется в лечении рака простаты. Опухоли в тканях замораживаются и разрушаются. Вариант применения холода используется для лечения рецидивов. При криотерапии предстательной железы очень тонкий датчик или игла из металла вводятся в предстательную железу через разрез между анальным отверстием и мошонкой. Для защиты мочеиспускательного канала одновременно через катетер подается теплый раствор соли.
Во время процесса применяется ультразвук – хирург смотрит на экран, подает внутрь жидкий азот или газ аргон, замораживает раковые ткани. За счет удаления тепла из предстательной железы клеточные мембраны разрываются, клетки погибают. После разрушения тканей лейкоциты убирают мертвые остатки, активизируется дополнительная иммунотерапия. Криотерапия предстательной железы имеет преимущества в виде неинвазивного характера, отсутствием общего наркоза, меньшей потери крови, быстрого восстановления, меньшего отека.
Брахитерапия
Подразделом лучевой терапии является лечение брахитерапией рака предстательной железы. Эта разновидность относится к низкоэнергетическому типу. Суть процедуры состоит в имплантации внутрь опухоли предстательной железы малых радиоактивных устройств – «семян». Они вводятся через кожу промежности при помощи специальной иглы, работают внутри простаты несколько месяцев, постоянно излучая.
К преимуществам брахитерапии предстательной железы относятся минимальная инвазивность, состояние сохранения органа, точная доставка, возможность дозировать облучение, снижение вероятности импотенции, быстрое восстановление. Побочными эффектами процедуры считаются дискомфорт при мочеиспускании, для решения проблемы можно установить катетер на срок до месяца. Брахитерапия может сочетаться с дистанционной лучевой терапией.


































Главное меню
Главное меню
Новые малоинвазивные технологии лечения рака предстательной железы
Рак предстательной железы (РПЖ) сегодня в Российской Федерации относится к числу самых быстрорастущих злокачественных новообразований. С каждым годом растет число больных с локализованным РПЖ − в прошлом году их было 44% от числа всех пациентов с впервые выявленным диагнозом опухоли предста-
тельной железы (Чиссов В.И., 2010). К основным или стандартным методам лечения сегодня относятся радикальная простатэктомия (РПЭ), брахитерапия (БТ), дистанционная лучевая терапия (ДЛТ), гормональная терапия (ГТ). Известны как хорошие отдаленные результаты этих методов, так и те осложнения, которые имеет каждый из этих методов:
- возможные осложнения РПЭ: недержание мочи, импотенция, стриктуры уретры, тромбоэмболические осложнения, лимфостаз и др.;
- возможные осложнения ДЛТ: ректиты, циститы, энтероколиты, стриктуры, импотенция, недержание мочи и др.;
- возможные осложнения БТ: ирритативные симптомы, стриктуры уретры, кишечные симптомы, импотенция и др.;
- возможные осложнения ГТ: приливы, импотенция, гинекомастия, остеопороз, сахарный диабет, кардиоваскулярные, гастроинтестинальные осложнения и др.
Новые взгляды на лечение РПЖ
В связи с наличием осложнений лечения именно у больных локализованным РПЖ с низким риском прогрессирования достаточно популярна – пока не в России, а за рубежом – тактика отсроченного лечения или тщательного наблюдения. Отсроченное лечение (Wirth M. et al., 2010) возможно при:
- ПСА ≤ 10 нг/мл;
- показателе Глисона ≤ 6;
- сТ1с-Т2а;
- числе позитивных биоптатов ≤ 2;
- ≤ 50% опухоли в биопсийном столбике.
Однако, риск прогрессирования заболевания, который иногда сложно оценить, несмотря на существующие номограммы, таблицы и группы прогноза, и психологический дискомфорт пациента с установленным диагнозом, но не получающим лечения, серьезно затрудняют применение этого метода в клинической практике.
При проведении динамического наблюдения очень сложно определить момент, когда следует переключиться с активного наблюдения на активное лечение. Перед урологом встают трудные вопросы: надо ли учитывать период удвоения ПСА менее 3 лет, снижение степени дифференцировки, увеличение градации по Глисону более 6 при повторных биопсиях, появление симптоматики (Wirth M. et al., 2010). Не всем из этих больных можно в последующем применить радикальное лечение ввиду по- жилого возраста и наличия сопутствующих заболеваний. После применения методов радикального лечения (РПЭ и ДЛТ) у части больных может развиться местный рецидив заболевания.
По нашему мнению, именно в этих двух группах пациентов с локализованным процессом и низким риском прогрессирования, и у больных с местным рецидивом опухоли после радикального местного лечения, показаны методы фокальной (аблятивной) терапии.
Применение методов фокальной терапии обеспечивает и радикальное излечение, и минимизацию побочных эффектов, которыми характеризуются стандартные радикальные методики, а именно – РПЭ и лучевая терапия (Lecornet et al., 2010).
Фотодинамическая терапия рака предстательной железы
В основе метода фотодинамической терапии лежит применение фотосенсибилизаторов, с последующим проведением светового облучения ткани предстательной железы через оптические световоды. Под воздействием лазерного излучения фотосенсибилизатор, введенный в ткань предстательной железы, вызывает ряд реакций, которые ведут к активизации процесса перекисного окисления, что, в свою очередь, приводит к:
- прямому некрозу опухолевых клеток за счет высвобождения свободных радикалов кислорода;
- нарушению микроциркуляции в капиллярах и развитию ишемического некроза;
- развитию местного иммунного воспаления, которое также потенциально может приводить в последующем к эффекту абляции опухоли (Moore CM et al., 2008).
В таблице 1 приведено несколько клинических наблюдений по проведению фотодинамической терапии у больных РПЖ.
Moore CM et al. (2008) Photodynamic therapy for prostate cancer—areview of current status and future promise
Первое поколение фотосенсибилизаторов отличалось длительным периодом экспозиции. Механизм действия второго поколения сенсибилизаторов, которые применяются в настоящее время, основан на сосудистых эффектах, поэтому время экспозиции исчисляется минутами. В разных исследованиях лазерному облучению подвергался различный объем (половина, вся железа, резидуальные ткани после ТУР) предстательной железы. Период наблюдения в этих работах очень небольшой, в основном, авторы исследовали токсичность данного метода, переносимость различных доз вводимых препаратов и доз мощности подводимого лазерного излучения.
Несмотря на то, что в некоторых публикациях осложнений вообще не наблюдалось (Zaak, 2003), у ряда авторов описаны достаточно серьезные осложнения, вплоть до развития ректоуретральных свищей, острой задержки мочеиспускания, и даже сепсиса (Weersink, 2005, Trachtenberg, 2008). Такие различия связаны с применением различных доз препаратов и мощности светового воздействия.
Собственный опыт
Методика фотодинамической терапии состоит во введении фотосенсибилизатора за несколько часов или за несколько минут досле операции. Интра — и послеоперационных осложнений зафиксировано не было. Дозы, которые мы использовали, пока еще, наверное, не достигли оптимальных значений.
Снижение уровня ПСА больше чем на 50% отмечено у 10 больных – по 5 в каждой группе при рецидивных опухолях и при перви чно выявленных. Средний уровень ПСА до начала лечения составлял 7,5 нг/мл, через шесть месяцев после фотодинамической терапии средний уровень был 3,4 нг/мл, через год – 3,1 нг/мл; медиана – чуть больше 2-х лет наблюдения.
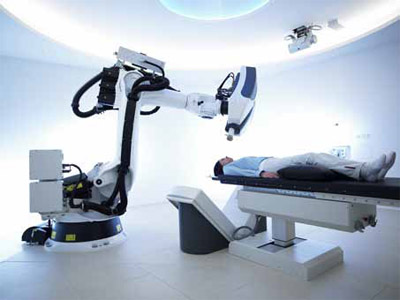
Рисунок 1. Кибер-нож
Ремиссия, которая определяется в виде отсутствия признаков как клинического, так и биохимического прогрессирования, наблюдалась у 37,5% больных. Биохимический рецидив или биохимическое прогрессирование диагностировано нами у 50% больных, но этих больных мы пока наблюдаем, т.к. скорость удвоения ПСА у них небольшая, имеется только биохимическое прогрессирование без развития клинического рецидива, и поэтому немедленную гормональную терапию мы пока не назначаем. Клинический рецидив, выявленный методами
лучевой диагностики, диагностирован только у 2-х пациентов. Один пациент умер от неопухолевой патологии.
Эффект совеременных ФДТ-препаратов основан на сосудистом воздействии, то есть на формировании микротромбов. В частности, это препарат «Тукад», механизм действия которого заключается в освобождении молекул оксида азота, расширяющих сосуды. Впоследствии наблюдается быстрое повреждение сосудистой стенки, формирование микротромбов в капиллярном русле и зоны ишемического некроза (Egeblad M. et al., 2010). Сегодня сосудисто-направленная фотодинамическая терапия считается одним из самых перспективных направлений в этой области.
Интересны результаты исследования II фазы PCM203, в котором приняли участие 85 пациентов. Лечение заключалось во внутривенной инфузии «Тукад» в дозе 4 мг/кг, трансперинеальном введении световодов и проведении сеанса ФДТ с мощностью излучения 200 Дж. Через 6 месяцев после сеанса пациентам выполняли биопсию, которая у 80% была негативной. Процент осложнений составил 6,2% (простатит, гематурия, орхит, стриктура уретры) (Azzouzi A. et al., 2011). Все эти осложнения достаточно быстро купировались в раннем послеоперационном периоде. Объем аваскулярной зоны, полученной в результате сеанса, был прямо пропорционален дозе облучения. Поэтому мы надеемся, что результаты ФДТ будут улучшены именно за счет увеличения дозы излучения.
Таким образом, сегодня фотодинамическая терапия является перспективным малоинвазивным методом лечения, который может быть проведен как у больных с низким риском прогрессирования, так и с местным рецидивом после лучевой терапии. Необходимы дальнейшие исследования токсичности и эффективности этой методики для более точного позиционирования ее в клинической практике.
Другие методы лечения РПЖ
Кибер-нож. Это высокоточная радиохирургическая система, которая представляет собой компактный линейный ускори-
тель с системой позиционирования и контроля изображения, что позволяет подводить более высокие дозы на минимальные объемы ткани. Сегодня этот аппарат используется, в основном, для лучевой терапии опухолей головного мозга – как первичных, так и метастатических (рисунок 1). Клинических данных по применению этого метода у больных РПЖ пока очень мало, они недостаточно изучены и отдаленные онкологические результаты отсутствуют.
Тем не менее, в 2011 г. опубликованы данные исследования, в
которое включены 67 больных локализованным РПЖ. При применении методики Кибер-ножа к опухоли подводилась большая доза излучения – пять фракций по 36 грей – всего 180 грей. Медиана наблюдения пока составляет 2,7 года – (King C., 2011). В конце 2,5-годичного периода наблюдения средний уровень ПСA составил всего лишь 0,5 нг/мл. Таким образом, безрецидивная выживаемость равнялась 94%.
Еще одна работа, с включением 55 больных локализованным РПЖ (Т1с-Т2с), касающаяся Кибер-ножа, была опубликована в 2011 г. (таблица 2).
Таблица 2. Распределение больных раком предстательной железы по стадии (ТNM), дифференцировки опухоли и степени прогноза
Лечение рака простаты





В отличие от аденомы, рак простаты – заболевание злокачественное. Особенность этой патологии – чувствительность опухоль к тестостерону и другим мужским гормонам. Это наиболее распространенное среди мужчин онкологические заболевание, часто имеющее типичную предысторию – простатит, аденома, рак. Несмотря на довольно медленное развитие, болезнь очень опасна.
 Причина тому – скрытное ее протекание. Развитие болезни происходит медленно и почти бессимптомно, поэтому часто выявляется уже в момент развития метастазов в печени, легких, костных тканях. Медицинская статистика, убедительно доказывает связь заболевания с концентрацией гормона тестостерона и возрастом пациента. Если в возрасте до 35 лет, рак предстательной железы выявляют у одного мужчины на 10000 то, со старением, риск заболеваний увеличивается в десятки и сотни раз. Так, у шестидесятилетних мужчин этот недуг наблюдают у каждого сотого, а у семидесятипятилетних, у каждого восьмого. Тестостерон не только стимулирует клеточный рост железы, но и возникшая опухоль тоже инфильтрируется под его влиянием. В норме, тестостерон может иметь три вида показателей:
Причина тому – скрытное ее протекание. Развитие болезни происходит медленно и почти бессимптомно, поэтому часто выявляется уже в момент развития метастазов в печени, легких, костных тканях. Медицинская статистика, убедительно доказывает связь заболевания с концентрацией гормона тестостерона и возрастом пациента. Если в возрасте до 35 лет, рак предстательной железы выявляют у одного мужчины на 10000 то, со старением, риск заболеваний увеличивается в десятки и сотни раз. Так, у шестидесятилетних мужчин этот недуг наблюдают у каждого сотого, а у семидесятипятилетних, у каждого восьмого. Тестостерон не только стимулирует клеточный рост железы, но и возникшая опухоль тоже инфильтрируется под его влиянием. В норме, тестостерон может иметь три вида показателей:
- Общий тестостерон – 12 -33 нмоль/л;
- Свободный тестостерон – 4.5 – 42 пг/мл;
- Биологически активный тестостерон – 3.5 — 12 нмоль/л.
Ввиду такой статистики, огромную роль играет своевременное выявление заболевания, а для этого, особенно пожилым мужчинам, нужно регулярно проводить профилактические осмотры, с обязательным анализом крови на концентрацию ПСА. Одним из более точных результатов определения бессимптомного онкологического процесса в простате на сегодня, является именно ПСА. Он основывается на определение в сыворотке венозной крови опухолевого маркера, который имеет название – простатического специфичного антигена (ПСА).
Диагностика
 Для успешного лечения, врач должен четко представлять, с какой опухолью он имеет дело, каковы ее размеры, где находится очаг роста, есть ли метастазы и многое другое. Для этого, перед выработкой комплекса лечебных мероприятий, проводят широкое обследование пациента:
Для успешного лечения, врач должен четко представлять, с какой опухолью он имеет дело, каковы ее размеры, где находится очаг роста, есть ли метастазы и многое другое. Для этого, перед выработкой комплекса лечебных мероприятий, проводят широкое обследование пациента:
- Анализ крови на предмет концентрации специфического антигена – ПСА. Если анализ показывает значительное превышение нормального показателя ПСА, стоит основательно провериться на предмет аденомы или даже раковой опухоли;
- Анальное пальпирование железы – позволяет определить атипичный рост простаты и возникновение на ней подозрительных уплотнений;
- Ректальное ультразвуковое исследование – показывает локализацию, размеры и форму опухоли;
- Игольчатая биопсия – забор небольшого участка ткани опухоли для дальнейшего микроскопического исследования гистологической природы ее клеток;
- Радиологическое исследование – рентгенография;
- Магнитная и компьютерная томография – наиболее информативные из всех аппаратных методов исследования. Они позволяют с высокой степенью достоверности уточнить размеры опухоли, тип ее роста и выявить, если таковые имеются, метастазы.
На основании полученных результатов ПСА и других обследований, определяют стадию развития болезни. Их четыре:
- 1 – начальная. На этом этапе, опухоль микроскопична и не диагностируема пальпацией и даже с помощью ультразвука. О ее присутствии может говорить завышенный уровень в крови ПСА;
- 2 стадия. На этом этапе, опухоль несколько больших размеров, однако не выходит за пределы простаты. При этом, она начинает подавать симптомы в виде проблем с оттоком мочи – вялое и затрудненное мочеиспускание, сопровождаемое резями. Уровень специфического антигена ПСА значительно возрастает, а это провоцирует активизацию ракового процесса. Возникают непривычные ночные позывы и ломота в костях. На этом этапе, опухоль можно обнаружить путем пальпации и УЗИ;
- 3 – развернутая. Разрастаясь, опухоль прорастает сквозь стенки простаты и поражает соседние ткани и органы. Отдаленные метастазы отсутствуют, но возможно поражение ими регионарных лимфоузлов. Для третьей стадии характерны – выделение мочи с кровяными вкраплениями, проблемы с потенцией, сильные боли при мочеиспускании и тянущие боли в области лобковой кости с радированием в поясницу;
- 4 – финальная. Развитие опухоли приводит к образованию сети метастазов в лимфоузлах, печени, легких, а в заключительном этапе, метастазы поражают костные ткани. Страдают преимущественно кости таза и кости спинного позвонка. Пациент сильно слабеет, теряет вес, страдает от сильных болей и постепенно угасает.
Если выявлена аденома – она лечится простым ее удалением, а терапия рака простаты, как и при любом другом онкозаболевании, состоит из традиционного набора методов – хирургия, химиотерапия, лучевая и гормональная терапии. В каждом отдельном случае, она подбирается индивидуально, в зависимости от состояния пациента, но общепризнанным, считается тот факт, что на ранних этапах, максимальную результативность дает хирургическое удаление опухоли с предоперационной лучевой подготовкой. Успешность лечения проверяют регулярным контролем антигена ПСА и радиологическими исследованиями.
Оперативное лечение
 Операция эффективна как для лечения аденомы, так раковой опухоли. Простатэктомия — удаление опухоли, проводят через разрез в брюшине или в области промежности. Совместно с аденомой, полностью удаляется также и вся железа, а если опухоль поздней стадии, то еще и часть соседних тканей, участок кости и пораженные лимфоузлы.
Операция эффективна как для лечения аденомы, так раковой опухоли. Простатэктомия — удаление опухоли, проводят через разрез в брюшине или в области промежности. Совместно с аденомой, полностью удаляется также и вся железа, а если опухоль поздней стадии, то еще и часть соседних тканей, участок кости и пораженные лимфоузлы.
Для уменьшения травматического эффекта и повышения качества результата, оперативное лечение рака простаты в Германии, например, проводят с применением медицинской робототехники, а лечение рака простаты в Израиле, благодаря новым эксклюзивным методам и новейшему оборудованию позволяет почти со 100% уверенностью гарантировать сохранение полноценной мужской потенции. Несколько хуже, дела обстоят в России, где высочайший уровень помощи, предоставляют только в лучших клиниках крупных городов – в Москве, Петербурге, Новосибирске и др.
Эффективность такого лечения, при условии, что опухоль ограничена пределами простаты и не проросла в ее стенки приближается к абсолютной, а вот в случае выхода опухоли за пределы железы и метастазировании в другие органы и кости, совместно с оперативным лечением применяют консервативные методы — химиотерапию и лучевую терапию.
Эти терапии могут применяться до операции и после. Предоперационная терапия служит для разрушения максимального количества раковых клеток и уменьшения таким образом опухоли, что существенно облегчает задачу хирургу, а послеоперационная, закрепляет полученные при операции результаты и снижает риски возникновения рецидива.
Терапия химическими препаратами
 Лечение проводят введением в организм химических лекарственных препаратов, обладающих избирательным воздействием – преимущественно на раковые клетки. Эти препараты убивают опухоль разрушая ядра составляющих ее клеток.
Лечение проводят введением в организм химических лекарственных препаратов, обладающих избирательным воздействием – преимущественно на раковые клетки. Эти препараты убивают опухоль разрушая ядра составляющих ее клеток.
Такое лечение, эффективно в развернутых стадиях болезни, когда хирургически удалить все пораженные клетки невозможно. В онкологических клиниках Москвы, активно применяется препарат Паклитаксел, который успешно уничтожает атипичные клетки с минимальным вредом для здоровых. Химиотерапевтическое лечение рака простаты в Израиле длится примерно 6 месяцев. При необходимости можно его повторить.
Лучевая терапия
 Лучевая терапия, представляет собой направленное облучение жесткими рентгеновскими лучами пораженного опухолью участка железы и узлов метастазов. Облучение повреждает структуру клеточной ДНК больных клеток, таким образом блокируя их размножение и останавливая развитие опухоли.
Лучевая терапия, представляет собой направленное облучение жесткими рентгеновскими лучами пораженного опухолью участка железы и узлов метастазов. Облучение повреждает структуру клеточной ДНК больных клеток, таким образом блокируя их размножение и останавливая развитие опухоли.
Для лучевой терапии применяют специальный аппарат – линейный лучевой ускоритель, который является источников гамма, бета или другого ионизирующего излучения, направленного на опухоль извне – дистанционного воздействия. Курс лучевой терапии продолжается два месяца, по пять 15 минутных процедур в неделю.
Более качественные результаты можно получить, если воздействовать на опухоль излучением, источник которого доставлен непосредственно в саму опухоль. Такой метод – брахитерапия, предусматривает игольчатое введение мельчайших радиоактивных частиц прямо в опухоль. По показаниям выбирают одну из разновидностей брахитерапии – временное введение радиоизотопов или введение их на постоянной основе.
Чаще всего, в лучевой терапии применяют изотопы цезия, иридия или радиоактивный йод, которые в результате воздействия на ткани опухоли разрушают их.
Лечение рака простаты в Германии успешно проводится и сравнительно новыми методами – терапия – HIFU. В этом методе, вместо радиологического облучения, раковые клетки подвергаются воздействию тонкого пучка лазера, который буквально их выжигает, разрушая их белковые соединения. Такое лечение рака простаты в Израиле считается наиболее перспективным и результативным.
Медикаментозное лечение
 Раковые клетки опухоли простаты, по большей части, гормонально чувствительны, особенно к тестостерону, а это значит, что гормоны, продуцируемые мужским организмом, в росте опухоли играют не последнюю роль. Поэтому, ведущие онкологические клиники, в том числе Российские – в Москве, разработали особый вид терапии — гормональное лечение рака простаты. Его роль сводится к подавлению выработки гормона и в результате этого снижению его концентрации в организме. В этом методе, применяют целый ряд лекарственных медпрепаратов:
Раковые клетки опухоли простаты, по большей части, гормонально чувствительны, особенно к тестостерону, а это значит, что гормоны, продуцируемые мужским организмом, в росте опухоли играют не последнюю роль. Поэтому, ведущие онкологические клиники, в том числе Российские – в Москве, разработали особый вид терапии — гормональное лечение рака простаты. Его роль сводится к подавлению выработки гормона и в результате этого снижению его концентрации в организме. В этом методе, применяют целый ряд лекарственных медпрепаратов:
- Гонадотропины – препараты, снижающие концентрацию тестостерона. К ним относят Фирмагон, Диэтилстильбэстрол и другие;
- Гипофизоподобные гормоны – Диферелин, Декапептил и подобные. Вызывают эффект кастрации – основные мужские гормоны перестают вырабатываться организмом;
- Противоандрогенные – Флуцином, Анандрон и подобные. Применяются в комбинации с гипофизными гормонами и позволяют добиться максимально полной андрогенной блокады.
Наиболее щадящим гормональным препаратом считается Касодекс, который даже без дополнительных медикаментов способен остановить рост опухоли, при этом он максимально щадяще действует на потенцию, оставляя ее в пределах нормы.
Аналог гормональной медикаментозной терапии – удаление яичек. Его применяют только в случае неэффективности медикаментозного гормонального лечения, когда уровень ПСА не удается снизить.
Виротерапия
 Среди самых передовых, почти экспериментальных методов лечения, отметим виротерапию. Она основана на действии специально модифицированных вирусов, которые «питаются» раковыми клетками.
Среди самых передовых, почти экспериментальных методов лечения, отметим виротерапию. Она основана на действии специально модифицированных вирусов, которые «питаются» раковыми клетками.
Наиболее востребованным виропрепаратом является ЕCHO 7 Rigvir. Он лучше других справляется с опухолью, а кроме этого, способствует восстановлению естественных иммунных свойств организма.
Справедливости ради, скажем, что такое лечение эффективно только в начальных стадиях развития болезни.
Нетрадиционное лечение
Лечение болиголовом. Болиголов – растение довольно ядовитое, однако в малых дозировках препараты на его основе приносят (по отзывам пациентов) существенный результат при лечении целого ряда заболеваний, в том числе рака простаты. Основные свойства болиголова – активизация общих иммунных процессов и клеточных, в частности.
Болиголов рекомендуют использовать для лечения всех типов опухолей в том числе и опухолей простаты. В этом случае советуют пользоваться настойкой болиголова, приготовленной исключительно из его цветов. Настойка болиголова принимается ежедневно, перед едой по чайной ложке. Для лучшего усваивания организмом, принимать настойку болиголова стоит, разведя разовую ее дозу в стакане воды.
Аконит Джунгарский. На территории России, лечение рака средствами из аконита занимает лидирующие позиции, наравне с болиголовом. Пациенты отзываются о средстве весьма положительно, однако считаем обязанностью предупредить – аконит, по силе действия, в десятки раз превосходит болиголов, поэтому дозировки аконита должны соблюдаться очень точно.
Настойку аконита готовят из порошка сушеных корней. Порошок настаивают в спирте, крепостью 60˚ в течение 3 недель, после чего процеживают через марлю. Пропорции, следующие 3 грамма аконита на 100 мл спирта.
- Дозировку и график приема настоек болиголова и аконита обязательно согласуйте с профессиональным фитотерапевтом, поскольку оба этих растения очень ядовиты и могут вызвать сильное отравление организма!
- Не лечите болиголовом и аконитом аденому и рак последней стадии, с метастазами в костных тканях – это может убить ваш организм преждевременно!
- И напоследок, стоит отметить, что традиционная медицина к такому лечению относится неодобрительно, кроме того, даже медицина Китайская, которая по праву считается наиболее осведомленной в целебных свойствах растений не говорит ни слова о пользе болиголова и аконита в лечении раковых заболеваний.
Источники: http://sovets.net/11915-lechenie-raka-predstatelnoj-zhelezy.html, http://ecuro.ru/article/novye-maloinvazivnye-tekhnologii-lecheniya-raka-predstatelnoi-zhelezy, http://rak03.ru/lechenie/lechenie-raka-prostaty/












































