Диагностика и лечение урологических осложнений рака предстательной железы
О. Асаад, В. В. Мешков
Клиника урологии и оперативной нефрологии РГМУ (зав. проф. Е.Б. Мазо), Москва, Россия
Одним из актуальных вопросов современной уроонкологии и урогериатрии продолжает оставаться рак предстательной железы (РПЖ). Увеличивающаяся в развитых странах продолжительность жизни, общемировая тенденция к старению населения обуславливают рост заболеваемости злокачественными новообразованиями, в т.ч. РПЖ. Ежегодно в пяти крупных странах Европы регистрируют 80000 новых случаев заболевания РПЖ и 45000 смертельных исходов, связанных с ним [50]. В России в 1992 г. РПЖ в структуре онкологической заболеваемости составил 2,9%, а в 1995 г. — уже 3,8%, в структуре онкоурологической заболеваемости — соответственно 36 и 41%. В целом за последние 10 лет частота РПЖ увеличилась в 2 раза [3]. Только в период с 1989 г. по 1996 г. число впервые диагностированных заболеваний выросло с 5,5 тыс. до 8,3 тыс., т. е. на 52 % [36].
Средний возраст больных РПЖ в России — 69 лет, а умерших — 70 лет; в США — 72 и 77 лет соответственно. В связи с особенностями клинического развития, опухоль может долгие годы не сказываться на самочувствии больного и проявить себя только у 8-10% заболевших, при этом вероятность умереть от РПЖ снижается до 30% [36, 43].
За последние годы, благодаря внедрению в клиническую практику новых методов диагностики (ТРУЗИ, КТ, МРТ, исследование концентрации ПСА крови), значительно чаще стали выявлять заболевание на более ранних стадиях.
Тем не менее, 50-70% больных обращаются за медицинской помощью по поводу развившихся осложнений, обусловленных РПЖ [9, 18, 36].
В тоже время клинической классификации осложнений РПЖ в настоящее время не разработано, хотя, по нашему мнению, это позволило бы выработать единый подход к диагностике, а главное, к тактике оказания специализированной медицинской помощи этим больным с учетом фактора времени их выявления.
Нарушения мочеиспускания — самый распространенный симптом (60-80%) при РПЖ [34]. Причиной его является раковая обструкция. Под обструктивными формами РПЖ подразумевают такие формы роста опухоли, которые нарушают свободный отток мочи по мочевым путям:
— инфравезикальные (обструкция пузырно-уретрального отдела);
— суправезикальные (опухолевое сдавление тазовых отделов мочеточников);
— сочетание обоих типов обструкции [20].
При этом частота инфравезикальной обструкции, по сообщениям различных авторов, варьирует от 17 до 72%, суправезикальной обструкции — от 2 до 51%. [51, 55]
Патогенез этих состояний при РПЖ многосторонен и включает не только механический фактор -сдавление и изменение уретро-везикального угла. К обструкции приводят также и расстройства кровообращения в системе тазовых вен на фоне хронического воспаления предстательной железы.
Процесс опорожнения мочевого пузыря также подвергается своеобразным изменениям. Для обеспечения мочеиспускания детрузорный компонент процесса может усиливаться с развитием гипертрофии, а затем прогрессивно и неадекватно снижаться, создавая условия для суб- и декомпенсации с появлением и увеличением количества остаточной мочи [4, 7].
Инфравезикальная обструкция в области пузырно-уретрального сегмента может быть следствием наличия как механического фактора — доброкачественная гиперплазия и РПЖ, так и динамического, обусловленного повышенным тонусом гладких мышц шейки мочевого пузыря, заднего отдела уретры и простаты [1, 7, 50]. Клинические наблюдения свидетельствуют, что при РПЖ обструкция пузырно-уретрального сегмента прогрессирует намного быстрее, чем при других патологических состояниях, приводящих к инфравезикальной обструкции [7].
Общепризнанно, что лечение больных с инфравезикальной обструкцией должно начинаться как можно раньше, еще до возникновения осложнений болезни. Поэтому, весьма важным является раннее ее выявление. Это необходимо и для установления этиологического диагноза, и для определения тактики лечения больных [2].
Постепенное или резкое снижение функциональных резервов детрузора может привести к развитию острой задержки мочеиспускания [7]. По данным Маринбаха Е.В., это состояние отмечается у 20% больных с РПЖ [34]. Симонов В. Я. и Козлов В. А. наблюдали острую задержку мочи у 12% пациентов этой категории [33]. По наблюдениям Аляева Ю.Г. и соавт. острая задержка мочеиспускания, которая может быть первым симптомом рака предстательной железы или возникнуть на фоне его лечения, возникает в 15-20% случаев [3]. Катетеризация мочевого пузыря, в этих ситуациях, может привести к восстановлению мочеиспускания или переходу в фазу хронической задержки мочи [7, 31]. При этом, на фоне снижения сократительной способности детрузора постепенно нарастает количество остаточной мочи и нарушение функции верхних мочевых путей.
Множество наблюдений свидетельствуют о том, что обструкция нижних мочевых путей, кроме дизурических расстройств, приводит к нарушению уродинамики верхних мочевых путей (мочеточников, почек) [54]. Зубко В. И. указывает на очень высокую степень развития этих нарушений (53,2%), наиболее частым из которых является одно- или двусторонний уретерогидронефроз [22].
Гидронефроз и уретерогидронефроз обычно развиваются бессимптомно. Однако, при анализе секционных карт умерших от РПЖ пациентов гидронефроз встречался в 9,7% случаев [45]. Клинических признаков, характерных только для этих состояний, нет [25, 30, 42]. Поэтому для уточнения состояния верхних мочевых путей необходимо применить методы диагностики, подтверждающие диагноз, определяющие причину его возникновения, выяснение стадии развития. Одним из первых должно быть проведено ультразвуковое исследование [30]. Оно дает возможность определить размеры лоханки и чашечек — степень их расширения и толщину паренхимы. Комбинация УЗИ с экскреторной урографией и радиоизотопной нефросцинтиграфией составляет первую группу стандартного урологического обследования больного, с помощью которого можно получить качественную информацию об имеющихся функциональных расстройствах [11, 39].
С помощью комбинации различных методов можно дать ответ на основные диагностические вопросы, связанные с характеристикой уродинамических расстройств, а именно: определить характер нарушения (обструктивный или динамический), выявить локализацию и гидродинамическую значимость имеющегося препятствия, а также охарактеризовать выраженность функциональной недостаточности и определить функциональные резервы верхних мочевых путей.
Это особенно важно в связи с тем, что уростаз и нарастающая дилатация верхних мочевых путей влечет за собой снижение кровенаполнения почечной коры и венозный стаз в медуллярной зоне [7]. Подобная перестройка в условиях хронической задержки мочеиспускания опасна развитием воспалительного процесса — пиелонефрита [22, 24]. Многие авторы указывают на возможность развития хронического пиелонефрита при бесконтрольном применении или использовании ударных доз эстрогенов, вызывающих дистрофические изменения в почках [21,43] и снижение тонуса мочеточников [5]. Лейзеруков Е. М. наблюдал признаки пиелонефрита у 71% больных, получающих эстрогенотерапию по поводу РПЖ, в то же время у 50% из них отмечалось расширение верхних мочевых путей [28]. По данным Самсонова В.А. среди осложнений РПЖ пиелонефрит встречается в 51,7% случаев [45]. Автор указывает, что этот инфекционный процесс обычно имеет колибациллярную этиологию. Отличительными особенностями хронического пиелонефрита у больных с инфравезикальной обструкцией и нарушением уродинамики верхних мочевых путей являются стойкое клиническое течение, частое рецидивирование, устойчивость к антибактериальной терапии [53]. Активный инфекционно-воспалительный процесс в мочеполовых органах при хирургическом вмешательстве создает предпосылки к развитию кровотечений, септических реакций (причина 4,8% всех летальных осложнений РПЖ [45]), тромбоэмболий (в 2,8% случаев смерти от РПЖ [45]), а также недержанию мочи [14].
Хронический пиелонефрит является одной из основных причин инвалидизации урологических больных вследствие развития в основном хронической почечной недостаточности, доля которой составляет 21-25% [15], вплоть до уремии [30]. При анализе секционных карт в исследованиях Самсонова В.А. отмечено, что уремия явилась результатом пиелонефрита и гидронефроза в каждом четвертом случае РПЖ [45].
Следует отметить, что часть больных, обращающихся за медицинской помощью по поводу урологических осложнений, уже имеют верифицированный диагноз РПЖ, а, возможно, и получали какой-либо из видов лечения. В этом случае важным представляется наличие диагностического алгоритма обследования этих больных. Однако, большинство (50-70%) составляют больные с неверифицированным диагнозом РПЖ. В этом случае описанные урологические нарушения требуют также этиологической диагностики для выбора правильной тактики комплексного лечения. Данные анамнеза и обследования дают основание заподозрить РПЭЖ как одну из причин описанных проявлений.
При возникновении подозрения на РПЖ в первую очередь принято проводить три необходимых обследования:
1. Пальцевое ректальное исследование. Специфичность метода составляет, по данным Матвеева Б. П., 37,9% [36], Хурсевича Н. А. и соавт. — 10,7% [46].
2. Определение уровня концентрации ПСА крови имеет наименьшее количество ложно-отрицательных результатов и наибольшую специфичность. Увеличение уровня ПСА до больших значений (около 20 нг/мл и выше) является высокоспецифичным даже при нормальных показателях ректального исследования [18, 27].
3. Трансректальное ультразвуковое исследование предстательной железы. Специфичность метода при диагностике РПЖ составляет 20-30% [36]. В исследованиях, проведенных Громовым А., показатели эффективности ультразвукового исследования в диагностике РПЖ составили: чувствительность — 70,2%, специфичность — 98,4%, точность — 98,1%, прогностичность положительного результата — 43,4% [17]. Хурсевич Н.А. и соавт. установили степень информативности метода ультразвуковой диагностики на уровне 27,7% [46]. Применение допплеровских методик в сочетании с трансректальным исследованием дает дополнительную информацию для выявления опухоли предстательной железы [29, 48].
Особое место в диагностике РПЖ занимает морфологическое подтверждение диагноза, основанное на исследовании материала полученного при биопсии. Благодаря оптимальному сочетанию низкой травматичности и информативности наиболее распространённой методикой является пункционная биопсия предстательной железы.
Показаниями к выполнению пункционной биопсии в настоящее время являются:
Несмотря на многостороннее обследование, получаемые данные часто противоречивы. Следует выработать алгоритм диагностики и комплексный подход к оценке результатов, а также оценить место и необходимость проведения каждого из методов обследования при урологических осложнениях РПЖ. Зубков А.Ю. с соавт. в качестве первого этапа диагностического алгоритма у больных с симптомами нарушения мочеиспускания предлагают определять уровень ПСА [23]. На втором этапе, по мнению авторов, всем пациентам должно проводиться пальцевое ректальное исследование и ТРУЗИ для избежания технической ошибки при определении концентрации ПСА крови. В дальнейшем в зависимости от показателей ПСА, данных пальцевого ректального исследования и ТРУЗИ производится многофокусная биопсия у центральной, периферической и переходной зон каждой доли предстательной железы с целью морфологической верификации диагноза РПЖ. Больным с повышенным уровнем ПСА (до 10 нг/мл) при наличии инфравезикальной обструкции авторы рекомендуют проведение трансуретральной резекции (ТУР) предстательной железы с диагностической и лечебной целью [23].
Комплексное применение диагностического алгоритма значительно повышает качество диагностики этиологической причины урологических осложнений и улучшает результаты лечения. Однако, такой подход требует дальнейшей разработки, уточнения и дополнения с целью его совершенствования и сокращения сроков оказания специализированной помощи больным.
Лечебная тактика при РПЖ, осложненном задержкой мочеиспускания, которую в настоящее время обсуждают в литературе, и определяет прогноз, длительность ремиссии, социальную адаптацию пациента.
Поскольку нарушения уродинамики нижних мочевых путей являются причиной большинства других осложнений РПЖ, вопросы их ликвидации представляют максимальный интерес.
В настоящее время в хирургическом лечении РПЖ с выраженными расстройствами мочеиспускания имеется три вида наиболее распространенных оперативных вмешательств:
1. радикальная простатэктомия;
2. трансуретральная криодеструкция;
3. трансуретральная или чреспузырная электрорезекция предстательной железы [42].
В случае впервые возникшей острой задержки мочеиспускания при подозрении на РПЖ Аляев Ю.Г. и соавт. рекомендуют дренировать мочевой пузырь по уретре мочеточниковым катетером № 6 по Шарьеру [3]. Это обеспечивает постепенную эвакуацию мочи, тем самым создает покой детрузору, восстанавливает его тонус, позволяет избежать быстрого развития гнойного уретрита как следствия ишемизации стенок уретры давящим катетером и присоединения инфекции. Дренирование мочевого пузыря позволяет провести комплексное обследование, цель которого — определить распространенность процесса. Однако, длительность дренирования лимитирована, это требует быстрой выработки дальнейшей лечебной тактики. Наличие уже развившегося уретрита не позволяет применять дренажные трубки. Невозможность дренирования в следствие генерализации опухолевого процесса со сдавлением уретры, резко сниженные функциональные способности детрузора, дилатация чашечно-лоханочной системы и хроническая почечная недостаточность рассматриваются авторами как показания к цистостомии, которая также является паллиативным вмешательством.
Ревунов А.Ф. и Карташов Е.М. предлагают при опухолях нижних мочевых путей, осложненных уретерогидронефрозом и пиелонефритом, проводить двухэтапное лечение: на I этапе — пиелонефростомия с оставлением в лоханке модифицированного скользящего дренажа для непрерывного орошения лекарственными препаратами, а после купирования воспалительного процесса — II этап оперативного вмешательства для восстановления мочеиспускания [44]. В случае локализованного РПЖ возможно выполнение радикальной простатэктомии. Однако, единого мнения о сроках ее проведения нет.
Для восстановления пассажа мочи по мочеиспускательному каналу наиболее часто применяют трансуретральная электрорезекция (ТУР) опухолевой ткани [14, 18, 41]. Существуют противоречивые мнения о возможности и оправданности применения ТУР при РПЖ. При этом в качестве контраргументов выступают такие факторы, как наличие сомнений в абластичности процедуры и практически полное сохранение периферической зоны предстательной железы, являющейся источником 70% очагов РПЖ [32]. Так, Лопаткин Н.А. с соавт. считают, что при инфравезикальной обструкции, острой задержке мочи и парадоксальной ишурии, вызванных РПЖ, оправдана консервативная тактика: осуществление адекватного дренирования мочевого пузыря, назначение гормональной терапии на 1-3 мес, с последующей попыткой восстановления самостоятельного мочеиспускания. И только в случае неудачи — ТУР. Авторы утверждают, что при таком подходе у 30-40% больных отпадает необходимость в отсроченном лечении [32];
В исследованиях Борщ В.Ю. и соавт. показаниями к ТУР являлись: неразрешающаяся самостоятельно острая задержка мочи; непереносимость надлобкового дренажа; инфравезикальная обструкция с выраженной дизурией и стремление избежать эпицистостомии. При сравнении годичной выживаемости в группе больных, перенесших ТУР, и контрольной группе (78 и 74%, соответственно) оказалось, что ТУР предстательной железы не приводит к значительному прогрессированию РПЖ в течение года наблюдения [8]. Это мнение подтверждают и данные, полученные Доброхотовым М.А.: единственным фактором, влияющим на продолжительность жизни больного, является стадия процесса и степень злокачественности РПЖ [19]. Поэтому авторы считают, что при наличии обоснованных показаний выполнение ТУР предстательной железы у данной категории больных обосновано. По мнению исследователей, при установленном диагнозе РПЖ необходимо руководствоваться следующими соображениями: для успешного устранения инфравезикальной обструкции и повышения эффективности последующего консервативного лечения удалить максимально возможное количество опухолевой ткани, но при этом не выйти за капсулу, не повредить замыкательный аппарат мочевого пузыря, что возможно при нарушении опухолью нормальных анатомических ориентиров [8, 35]. Варенцов Г.И. и соавт. указывают на целесообразность активной тактики при задержке мочи, вызванной РПЖ: одним из этапов комбинированного лечения должно быть одномоментное эндоскопическое оперативное лечение (ТУР). Данное малотравматичное вмешательство позволяет получить материал для морфологического исследования, улучшить уродинамику, остановить кровотечение. Такая тактика улучшает качество и продолжительность жизни у этой категории больных. Средняя продолжительность жизни в данном наблюдении составила 3,5 года (11 мес — 4,5 года) [12]. При этом Чеченин М.Г. и Робустов В.В. рассматривают ТУР как операцию, которая может быть выполнена по срочным показаниям, и является методом выбора [47]. Многие исследователи указывают на то, что использование ТУР позволяет свести до минимума выполнение инвалидизирующих операций по внеуретральной деривации мочи (цистостомия, уретеропиелонефростомия) [20, 38]. Мартов А.Г. и Гущин Б.Л. указывают на эффективность этого метода и при ликвидации кровотечения из расширенных вен предстательной железы [35]. В целом, по мнению многочисленных авторов, данная операция направлена, главным образом, на улучшение качества жизни больного с целью избавления его от пожизненно наложенной эпицистостомы и удлинение сроков жизни за счет такого морального фактора, как восстановление нормального мочеиспускания и применения антиандрогенов и эстрогенов [8,16,19,38]. При этом, по данным Гориловского Л.М. и Доброхотова М.А., осложнения ТУР наблюдаются в 12,7-13,8%, летальный исход — в 3,4% случаев [16, 19].
Накопленный урологами опыт криодеструкции и особенно трансуретральной резекции РПЖ показывает безусловную целесообразность частичного удаления опухоли для восстановления чрезуретрального мочеиспускания. Кроме того, в связи с уменьшением массы опухоли было показано повышение эффективности эстрогенотерапии после ТУР [20]. После такой резекции РПЖ и восстановления мочеиспускания антиандрогенная терапия длительно поддерживает удовлетворительное состояние больных, освобождая их от надлобкового дренажа [41]. Важно и то, что ТУР опухолевой ткани предстательной железы приводит к некоторым иммунологическим сдвигам в организме больных. Так, на 7-е и 15-е сутки после проведения ТУР в сыворотке крови отмечается резкое повышение титров антител против ткани предстательной железы (1:126 — 1:256) по сравнению с их содержанием до проведения оперативного вмешательства (1:4 -1:16). Можно предположить, что при этом повышается толерантность иммунной системы к опухолевой ткани предстательной железы [14].
Хотя ТУР широко применяется в настоящее время, но единого подхода к этому методу лечения не выработано. Поэтому, по-прежнему, актуальным остается вопрос разработки использования ТУР в лечении нарушений мочеиспускания при РПЖ. Важно также разработать четкие показания и последовательность выполнения различных лечебных манипуляций.
Наряду с этим, многие клиницисты говорят о необходимости предоперационного гормонального лечения, т. н. неоадъювантной терапии. Результатом неоадъювантной терапии является снижение стадии РПЖ, локальное ограничение процесса, уменьшение болезненности и последствий операции, замедление прогрессии и удлинение выживаемости больных [13]. Андрогенная депривация в виде максимальной андрогенной блокады (орхэктомия + антиандрогены) в исследовании Когана М.И. с соавт. приводила к заметному ускорению восстановления функции наружного сфинктера по удержанию мочи при сравнении с теми, кому такая подготовка не проводилась [26]. Однако, до сих пор четко не определены необходимость, показания, режим назначения неоадъювантной терапии в комплексе лечения РПЖ. Место орхэктомии исследовал Бухаркин Б.В. Автором доказано, что этот метод не влияет на продолжительность жизни и не может быть обязательным компонентом комплексного лечения [10].
При уродинамических нарушениях с гидронефрозом Бегаев А.И. и соавт. проводили дополнительное наружное дренирование мочеточников во время операции [6]. По мнения Петрова С.Б. и Бабкина П.А. изменения мочевыводящих путей (гидронефроз, гидроуретеронефроз) с развитием почечной недостаточности требуют одно- или двусторонней нефростомии и комбинированной терапии хронической почечной недостаточности, а в дальнейшем лечения антиандрогенами [40]. На основании наблюдений Лопаткина Н.А. и соавт. нефростомия абсолютно показана в тех случаях, когда гидронефроз осложнен пиелонефритом. По мнению авторов, дренировать почку следует 2-3 нед до восстановления адекватного пассажа мочи и уменьшения выраженности пиелонефрита [30].
Перспективным направлением в лечении задержки мочи, в том числе с развитием гидронефротической трансформации, является применение уретральных стентов. В исследовании, проведенном Yachia D. и Aridogan J.A., спонтанное мочеиспускание восстановлено в 55% случаев применения уретральных стентов при раковой обструкции, и эффект сохранялся от 3 до 48 мес после их удаления [56]. По данным Gottfried H.W. и соавт. симптомы обструкции разрешились у 94% пациентов с РПЖ, результат был неизменен в течение в среднем 15,2 мес (от 3 до 38 мес) [52]. Поэтому использование стентов является альтернативой трансуретральной резекции предстательной железы при инфравезикальной обструкции, вызванной раком. Anson K.M. и соавт. указывают на значительную эффективность и увеличение продолжительности жизни при комбинации стентов с андрогенсупрессивной терапией [49]. Это наименее инвазивное вмешательство особенно показано пациентам с впервые выявленным РПЖ с высоким риском оперативных вмешательств. Однако, проблема стентирования мочевых путей по-прежнему представляет большой практический интерес.
Таким образом, несмотря на то, что урологические осложнения РПЖ хорошо известны, до настоящего времени нет их комплексной оценки: отсутствует клиническая классификация этих осложнений, их специфическая (онкологическая) симптоматика, алгоритм диагностики и обоснованная тактика лечения с учетом факторов времени выявления, выбора метода вмешательства, а также показания и противопоказания как к оперативным, так и консервативным методикам для улучшения качества жизни этой тяжелой группы больных. Эти обстоятельства и обусловливают актуальность выбранной темы.
Мочеиспускание и моча при раке простаты

-
Содержимое:
- Непроходимость мочи
- Частое мочеиспускание
- Кровь в моче при онкологии простаты
- Влияние рака простаты на цвет мочи
- Запах мочи и онкология простаты
При развитии онкозаболевания предстательной железы наблюдается обструкция мочевого пузыря и сдавление уретрального канала. По мере развития патологических изменений, метастазы прорастают в ближайшие органы, что отражается на работе мочеполовой системы.
Моча при раке простаты – важный диагностический фактор. Непроходимость, произвольные подтекания, гематурия – все эти проявления учитываются во время дифференциальной диагностики заболевания.
Как онкология простаты влияет на мочевой пузырь
Рак простаты долгое время развивается практически бессимптомно. Зачастую, проблемы с мочеиспусканием в любом проявлении – первый тревожный сигнал, который нельзя оставлять без внимания.
Опухолевый процесс онкозаболевания проявляется следующей симптоматикой:
- Рези и жжение при мочеиспускании.
- Частые ночные позывы в туалет и ощущение неполного опорожнения мочевого пузыря.
- Изменение цвета и запаха.
- Появление примесей в виде хлопьев и небольших сгустков.
Появление любого из перечисленных симптомов, тревожный сигнал организма, указывающий как на онкологию, так и на другие патологические изменения.
Только после полного обследования организма, врач назначит курс лечения с целью облегчить мочеиспускание и уменьшить болевой синдром. Самостоятельное лечение недопустимо.
Последствия задержки мочи: нарушение в работе почек, развитие воспалительных процессов в мочеполовой системе.
Наибольшую опасность вызывает ситуация, когда первые нарушения мочеиспускания попросту игнорируют. Больной принимает анальгетики и спазмолитики, чтобы облегчить боль, что приводит к кратковременному улучшению самочувствия. При возвращении симптоматики и обращению к врачу у пациента обычно диагностируют рак в запущенной стадии, тяжело поддающийся лечению.
Мочеиспускание может сопровождаться болью и при доброкачественном новообразовании. Точный диагноз поставит лечащий врач после проведения ряда анализов и исследований.
Непроходимость мочи

Курс, направленный на снижение симптоматики следующий:
- Стентирование мочевого пузыря — снижает нагрузку на простату и дает время для восстановления железы. Через дренаж при необходимости, пузырь промывают дезинфицирующими и антибактериальными растворами. Расширение мочеиспускательного канала происходит постепенно, по мере того как устраняется инфекционный и механический фактор. Цистома удаляется.
- Лечебная физкультура — упражнения были разработаны Кегелем – американским гинекологом. Высокая эффективность лечебной физкультуры привела к применению комплекса для лечения мужчин.
- Медикаментозная терапия — назначается курс антибиотиков и средств, восстанавливающих нормальный отток жидкости из организма. Лекарства назначаются с крайней осторожностью, исключительно по показаниям.
Частое мочеиспускание
Еще одна распространенная проблема при раке простаты частое мочеиспускание у мужчин. Проявление нарушений носит следующий характер:
- Частые ночные позывы в туалет.
- Ночное недержание.
- Непроизвольное подтекание мочи, вызванное механическими факторами: кашлем, чиханием, резким движением.
Симптоматика нарастает по мере разрастания онкологического заболевания и инфильтрации злокачественных клеток в мышечные ткани. Если у мужчины недержание мочи при раке предстательной железы происходит на фоне сделанной простатэктомии или другого хирургического вмешательства, негативные проявления проходят самостоятельно, спустя 1-2 месяца.
Кровь в моче при онкологии простаты
Периодические выделения крови при мочеиспускании указывают, что онкозаболевание перешло в 3-4 стадию. Опухоль начала прорастать в прямую кишку, мочевой пузырь, семенные пузырьки.
Сгустки крови в моче появляются и после проведенной простатэктомии. В этом случае симптоматика носит временный характер и не вызывает опасений.
При хроническом простатите, часто сопровождающем онкозаболевание, изменение цвета может вызывать гной в моче – следствие воспалительного процесса. В любом случае, появление посторонних примесей – повод сдать клинические анализы и обратиться к урологу за консультацией.
Забор образцов для исследований показывает следующее:
- Эритроциты в моче — показатели в норме не превышают 1-2 ед, и могут вообще не обнаружиться во время исследования. Повышенный уровень эритроцитов указывает на несколько нарушений, включая мононуклеоз – опухолевый процесс в почках.
- Повышение лейкоцитов — указывает на воспалительные процессы, включая разрушение тканей по причине разрастания раковых клеток.
Влияние рака простаты на цвет мочи
При раке простаты, изменение цвета и структуры мочи, еще один характерный симптом. В жидкость, отходящую из организма, попадает большое количество чужеродных вкраплений, что и влияет на появление нехарактерных оттенков:
- Мутная моча — характерный признак для онкологии, сопровождающейся сахарным диабетом и воспалением мочеполовой системы. В жидкости присутствуют хлопья, вкрапления. Симптом того, что в моче завышен белок.
Мутная консистенция с видимыми вкраплениями указывает на развитие опухолевых процессов вне простаты – почках и уретральном канале. - Темная и алая моча — указывает на гематурию. Разрушение тканей пузыря, семенных протоков, уретрального канала приводит к выделению крови внутри организма, сгустки пролабируют в моче.
- Пенистая консистенция.
При гиперплазии и онкологии простаты, во время мочеиспускания периодически выходят кусочки слизистой, что влияет на состав и консистенцию отходящих жидкостей. Необходима дифференциальная диагностика, чтобы точно определить, что является катализатором изменений.
Запах мочи и онкология простаты
В нормальных условиях моча имеет запах, без каких-либо оттенков. Появление патологических изменений сразу отражается на структуре жидкости.
При онкологии появляется резкий запах мочи, характерный для следующих состояний:
- «Аптечный» запах — если моча при мочеиспускании пахнет лекарствами, это прямое указание на развитие воспалительных заболеваний: пиелонефрита, почечной недостаточности. Возникает по причине увеличения кислотности мочи.
- «Рыбный» запах — сопровождает увеличение в концентрации гормонов надпочечников в крови. Указывает на развитие злокачественной и доброкачественной опухоли. Сильный запах мочи, один из характерных симптомов развития ракового заболевания простаты и разрастания метастаз.
Неприятный запах аммиака у пациентов с острыми задержками мочи начинает исходить от тела и наблюдается даже при соблюдении хорошей личной гигиены.
Может ли рак простаты прорасти в мочевой пузырь
Рак простаты и рак мочевого пузыря могут быть одновременно. Состояние развивается после начала метастазирования онкологии в ближайшие ткани.
Рядом с простатой расположены семенные пузырьки, прямая кишка, лимфоузлы и мочевой пузырь, почки. Поражение метастазами начинается в первую очередь с ближайших органов.

Синхронный рак мочевого пузыря и простаты наблюдается в 30-45% случаев и считается достаточно распространенным явлением. Об одновременном поражении свидетельствуют совокупность следующих анализов:
- Повышенные показания белка в моче.
- Устойчивая гематурия.
- Изменение состава и концентрации отходящей жидкости: плотности, цвета, появление неприятного запаха.
- Высокий сахар в моче связанный с глюкозурией, нарушением в работе почек.
Не всегда перечисленная симптоматика доказывает наличие рака. В некоторых случаях подобные клинические проявления характерны для:
- Сахарного диабета.
- Воспаления почек и уретрального канала.
- Доброкачественной гиперплазии.
Некоторые симптомы носят временный характер и проходят самостоятельно, например, после удаления рака хирургическим путем. От уролога-онколога требуется правильно поставить диагноз. Для этого назначают ряд инструментальных исследований. По результатам дифференциальной диагностики назначают паллиативное лечение.
После операции при раке простаты
 Сразу после операции при раке простаты
Сразу после операции при раке простаты
Сразу после окончания операции вас транспортируют в послеоперационную палату, где врач-реаниматолог будет следить за вашим общим состоянием, процессом пробуждения и восстановления сознания. На вторые сутки после операции вас переведут в вашу палату в отделении.
Дренаж после операции
В большинстве случаев в процессе операции хирург оставляет дренажyю трубку в полости малого таза (в зоне операции). Дренаж, располагаемый в ложе предстательной железы, необходим для оттока избыточной жидкости (лимфы) и крови, оставшейся или выделившейся в ране. В первые несколько дней по дренажу будет выделяться сукровица, как правило, к третьему-четвертому дню дренаж извлекается.
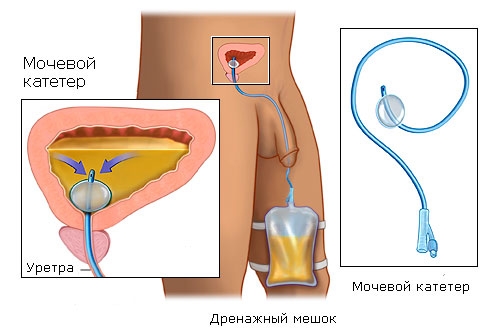
Мочевой катетер после операции при раке простаты
Мочевой катетер дренирует мочу из мочевого пузыря, предотвращая ее истечение через уретру, и тем самым создавая условия для ее быстрого заживления после операции по поводу рака простаты. Мочевой катетер присоединяется к дренажному мешку, в котором скапливается выделяемая моча из мочевого пузыря. Катетер из мочевого пузыря удаляется через 8-10 дней после операции. Иногда может потребоваться и больший период времени для заживления уретры (как правило после лучевой терапии), тогда ваш доктор скажет, что можно будет удалить катетер. В первые несколько дней после операции катетер может вызывать спазмы мочевого пузыря, дискомфортные ощущения внизу живота и ощущения необходимости помочиться. Со временем дискомфорт уменьшится. Как правило, после операции, мы выписываем домой пациента только тогда, когда уретральный катетер удален. Однако при желании пациента он может быть выписан и раньше с уретральным катетером. В этом случае при выписке врач объяснит вам, как ухаживать за мочевым катетером и дренажным мешком. Верхушку головки пениса, где выходит мочевой катетер, необходимо обрабатывать вазелиновым маслом хотя бы раз в день для предотвращения травм и микротрещин.
Более раннее извлечение катетера может повлечь за собой ряд осложнений, в том числе недержание мочи или, наоборот, острую задержку мочи.
Удалить катетер вы можете в поликлинике по месту жительства, но лучше обратиться за помощью к вашему оперирующему хирургу. Удаление катетера – безболезненная процедура, занимающая лишь несколько секунд.
После удаления мочевого катетера, необходимо некоторое время для того, чтобы ваш мочевой пузырь «вспомнил» как правильно функционировать. Со временем восстановятся функции мышц мочевого пузыря и контроль над актом мочеиспускания. К концу первого месяца после операции 60% мужчин восстанавливают полный контроль над актом мочеиспускания. К третьему месяцу после операции по поводу рака простаты функция мочевого пузыря и мышц тазового дна восстанавливается у 90% мужчин, а через 6 месяцев – у 92-95%.
Более быстрому восстановлению контроля над актом мочеиспускания помогут упражнения, направленные на укрепление мышц тазового дна, а именно упражнение Кегеля.
Упражнение Кегеля для укрепления мышц тазового дна
Они состоит из трех частей (медленного сжатия, сокращения и выталкивания):
Первый этап – медленное сжатие: во время выполнения этого упражнения необходимо медленно напрягать мышцы тазового дна, как вы это делаете обычно например для остановки мочеиспускания или дефекации. Удерживайте напряжение в течение 3-5 секунд. Расслабьтесь и повторите упражнение через 10 секунд.
Второй этап – сокращения: необходимо быстро напрягать и расслаблять мышцы промежности.
Третий этап – выталкивание: при выполнении упражнения необходимо потужиться как при мочеиспускании или дефекации.
Упражнение каждого этапа выполняется по 5-10 раз, а весь комплекс – 3-5 раз в день. Каждую неделю увеличивайте количество выполняемых упражнений на 5, пока количество повторений каждого упражнения не достигнет 30-40 раз.
 Болевой синдром после операции
Болевой синдром после операции
После операции при раке простаты вы можете испытывать боль или дискомфорт в области хирургического вмешательства. Для борьбы с болевым синдромом в условиях стационара используются как наркотические, так и ненаркотические аналгетики. Если во время анестезиологического пособия вам выполнялась эпидуральная анестезия с постановкой катетера, он может использоваться для продленного послеоперационного обезболивания.
В случае возникновения умеренной боли и дискомфорта в домашних условиях, вы можете использовать нестероидные противовоспалительные препараты, такие как ибупрофен, парацетамол и др. Длительность болевых ощущений в среднем может сохраняться до 14-20 дней после операции.
Сексуальная функция
 Операция может повлиять на вашу половую жизнь. Сексуальная функция заключается в достижении эрекции, эякуляции и оргазма. Во время эякуляции происходит выделение наружу семенной жидкости, большая часть которой вырабатывается в простате и семенных пузырьках. Поэтому после радикальной простатэктомии, в процессе которой удаляется простата и семенные пузырьки, во время эякуляции выделяется лишь незначительное количество эякулята или его может не быть вовсе. Как правило, операция не влияет на вашу возможность испытывать оргазм, даже несмотря на небольшое количество эякулята.
Операция может повлиять на вашу половую жизнь. Сексуальная функция заключается в достижении эрекции, эякуляции и оргазма. Во время эякуляции происходит выделение наружу семенной жидкости, большая часть которой вырабатывается в простате и семенных пузырьках. Поэтому после радикальной простатэктомии, в процессе которой удаляется простата и семенные пузырьки, во время эякуляции выделяется лишь незначительное количество эякулята или его может не быть вовсе. Как правило, операция не влияет на вашу возможность испытывать оргазм, даже несмотря на небольшое количество эякулята.
Эрекция происходит тогда, когда половой член наполняется кровью. Это происходит в ответ на стимуляцию нервных окончаний, расположенных в половом члене. Нервные сигналы распространяются по двум нервным пучкам, расположенным по обеим сторонам от простаты. Иногда в процессе операции данные нервы могут повреждаться. Однако даже сохранение целостности нервных пучков не всегда гарантирует восстановление эрекции после операции. Как правило, восстановление эрекции после операции по поводу рака простаты происходит намного медленнее, чем восстановление функции мочеиспускания. Среднее время восстановления эрекции составляет 6-18 месяцев, иногда затягиваясь на 2-3 года.
Существует несколько методов, которые могут помочь вам улучшить эрекцию, например, применение ингибиторов фосфодиэстеразы пятого типа, вакуум-эректорного приспособления и др. Как правило, их использование разрешается не ранее чем через 4-6 недель после операции.
К использованию этих методов следует прибегать только после консультации с вашим лечащим врачом.
Вы можете возобновлять половую активность после удаления мочевого катетера и заживления послеоперационной раны, и как только почувствуете, что ваша сексуальная функция полностью восстановилась.
К сожалению, в процессе операции нарушается сообщение между уретрой и семенными протоками, в результате чего сперматозоиды не могут выделяться наружу и участвовать в процессе оплодотворения – у мужчины развивается бесплодие.
 Послеоперационная рана
Послеоперационная рана
Очень важно после операции при раке простаты содержать рану в чистоте и сухости. В первые дни рану необходимо обрабатывать антисептическими растворами для предотвращения инфицирования. Швы снимаются через 7-14 дней после операции. Если края раны сшиты с помощью специальных скрепок (скоб), то их также необходимо удалять через 7-10 дней после операции, тогда как если применялся рассасывающийся шовный материал, то швы исчезнут самостоятельно к 10 дню после операции.
Антибактериальная терапия
 После радикальной простатэктомии врач назначит профилактический курс антибактериальных препаратов, которые вы начнете получать еще в стационаре. Для предотвращения развития инфекции мочевыделительной системы антибиотики необходимо принимать и весь период стояния катетера в мочевом пузыре. Иногда длительная антибиотикотерапия может провоцировать появление грибковой инфекции, проявляющейся воспалением в области мошонки. В этом случае можно использовать противогрибковые крема.
После радикальной простатэктомии врач назначит профилактический курс антибактериальных препаратов, которые вы начнете получать еще в стационаре. Для предотвращения развития инфекции мочевыделительной системы антибиотики необходимо принимать и весь период стояния катетера в мочевом пузыре. Иногда длительная антибиотикотерапия может провоцировать появление грибковой инфекции, проявляющейся воспалением в области мошонки. В этом случае можно использовать противогрибковые крема.
Дома после операции
Дома вы можете принимать душ на следующий день после выписки из стационара. Избегайте принятия ванн до момента удаления мочевого катетера.
Важно совершать ежедневные прогулки. Это не только ускорит процесс восстановления, но и предотвратит формирование тромбов в венах нижних конечностей.
Не стоит поднимать тяжести, как минимум 6 недель после операции, т.е. до полного заживления послеоперационных ран.
 Диета и функция кишечника
Диета и функция кишечника
По возвращении домой вы сможете питаться так же, как питались до операции. Однако не забывайте, что здоровое питание поможет вам не только сократить период восстановления после операции, но и максимально сохранить физическое здоровье.
Очень важно после операции избегать развития запоров. Для предотвращения запоров можно использовать различные препараты, например, лактулозу. Однако ни в коем случае нельзя выполнять клизму как минимум 4 недели после операции. Стенка прямой кишки, близкая к зоне операции, имеет большой риск повреждения в первые три месяца после хирургического вмешательства.
Безотлагательно обращайтесь к врачу в случае:
- высокой температуры;
- выраженного болевого синдрома, не устраняемого нестероидными противовоспалительными препаратами;
- неконтролируемой тошноты и рвоты;
- запоров, не проходящих после применения лактулозы;
- расхождения краев раны или возникновения признаков инфицирования (покраснения и припухания);
- проблем с мочевым катетером.
После операции вы будете постоянно находиться под наблюдением вашего лечащего врача. Послеоперационное наблюдение важно для ранней диагностики рецидива. Кроме того врач будет контролировать процесс восстановления функции мочеиспускания и половой активности. Послеоперационный мониторинг заключается в регулярном контроле уровня ПСА и выполнении пальцевого ректального исследования. На первом году после операции регулярные осмотры и тест на уровень ПСА проводятся один раз в три месяца, далее каждые шесть месяцев.
К сказанному добавим, что в своей практике мы никогда не выписываем пациента до удаления уретрального катетера. Данная процедура является очень важной после операции по удалению рака простаты. Более того, перед удалением мы всегда вводим контрастную жидкость в мочевой пузырь и проводим рентгеновское исследование. Только при полной целостности соустья между уретрой и мочевым пузырем катетер может быть удален. Еще сутки пациент находится под нашим наблюдением. Убедившись в том, что мочеиспускание полностью восстановлено, мы отпускаем пациента домой.
Источники: http://medi.ru/info/9712/, http://ponchikov.net/health/urologiya/612-mocha-pri-rake-prostaty.html, http://therapycancer.ru/rak-predstatelnoj-zhelezy/1299-posle-operatsii-pri-rake-prostaty













































