Диагностика рака предстательной железы
Глава 4. Диагностика рака предстательной железы
Тщательно собранный анамнез помогает установить некоторые особенности заболевания. Симптомы рака предстательной железы, особенно дизурия, развиваются быстро. Иногда постепенно ухудшается общее состояние, больной жалуется на слабость, похудание. Внешний вид пациента изменяется только при далеко зашедшем опухолевом процессе. Истощение и выраженная бледность кожи наблюдаются редко. При осмотре следует обращать внимание на состояние лимфатических узлов, печени, почек, мочевого пузыря, определять количество остаточной мочи. При возникновении подозрения на рак предстательной железы в первую очередь принято проводить три необходимых исследования:
I. Пальцевое исследование простаты.
II. Определение уровня простато-специфического антигена (ПСА).
III. Ультразвуковое исследование (УЗИ) простаты, при показаниях -одновременно с биопсией.
Пальцевое исследование прямой кишки. Пальцевое исследование прямой кишки — самый простой, дешевый и безопасный метод диагностики рака предстательной железы. Однако результаты исследования во многом определяются размерами опухоли и ее локализацией. Пальпация железы осуществляется в коленно-локтевом положении больного, либо при лежании на правом боку. В результате пальпации врач может выявить следующие симптомы опухоли предстательной железы.
1. Ассиметричная предстательная железа.
2. Плотной или деревянистой консистенции части предстательной железы. Плотность может определяться в виде отдельных узлов, либо различной величины инфильтратов, вплоть до перехода их на стенки таза.
3. Неподвижность железы вследствие сращения ее с окружающими тканями.
4. Пальпируемые семенные пузырьки.
Данные, полученные при пальпации, не всегда легко интерпретировать, так как ложно положительный диагноз рака предстательной железы возможно поставить при следующих обстоятельствах:
1. Доброкачественная гиперплазия предстательной железы.
2. Камни предстательной железы.
4. Флеболиты стенки прямой кишки.
5. Полипы или рак прямой кишки.
6. Аномалии семенных пузырьков.
Результаты пальпации безусловно очень трудно дифференцировать от перечисленных заболеваний, но зато они являются вескими основаниями для дальнейшего обследования больного. В среднем только у одной трети случаев пальпируемых узлов предстательной железы впоследствии гистологически верифицируют рак простаты.
Определение уровня простато-специфического антигена (ПСА). Поскольку простато-специфический антиген имеет большое значение не только для диагностики, но и для лечения и прогноза рака предстательной железы, более подробно остановимся на этом маркере.
В скрининговых программах традиционно используют пороговый уровень в 4 нг/мл для всех возрастных групп. Использование предложенного уровня снижает количество ложно-положительных определений при гиперплазии предстательной железы.
Уровень ПСА в сыворотке крови может быть повышен по следующим причинам:
— рак простаты,
— доброкачественная гиперплазия простаты,
— наличие воспаления или инфекции в простате,
— ишемия или инфаркт простаты,
— эякуляция накануне исследования.
Диагностическая значимость почти всех опухолевых маркеров ограничена из-за ложно-положительных значений, наблюдаемых при некоторых незлокачественных патологиях. Длительно ведутся споры о том, оказывает ли пальпаторное обследование предстательной железы влияние на уровень ПСА в сыворотке. Некоторые авторы (Brawer et аl., 1988) считают, что такого влияния практически нет, другие наблюдали значительные изменения в уровне маркера после массажа простаты, хотя и не во всех случаях (Stamey et аl., 1987). С другой стороны, несомненно, инвазивные методы (трансуретральная биопсия или трансуретральная резекция простаты) приводят к значительному повышению сывороточного уровня ПСА. Stamey с соавторами (1987) в детальном исследовании показали, что при массаже простаты концентрация ПСА в сыворотке крови через 5 минут увеличивалась в 1.5-2 раза, и наиболее высокой была у больных с клиническими признаками гипертрофии. У больных, у которых массаж комбинировался с цистоскопией, ПСА увеличивался в 4 раза, а сразу же после биопсии перинеальных лимфоузлов и трансуретральной резекции — в 50-60 раз.
Из незлокачественной патологии предстательной железы простатиты острые или хронические могут приводить к значительному повышению ПСА (Dalton et аl., 1989). Доброкачественные гиперплазии могут давать высокую частоту ложно-положительных результатов, причем экспрессия антигена зависит от величины железы (Eicoreetal., 1987; Hudson et аl., 1989). Так Stamey с соавторами (1987) показали, что уровень ПСА у группы больных с гиперплазией предстательной железы перед операцией варьировал от 0.3 до 37 нг/мл и превышал уровень в 2.5 нг/мл у 86% тех больных, у которых вес резицированной ткани был от 6 до 36 грамм. Подсчитано, что концентрация ПСА в сыворотке больных с гиперплазией предстательной железы составляет 0.31 -0.2 нг/г гипертрофированной ткани. Частота ложноположительных значений при гиперплазии предстательной железы при пороговом уровне 4нг/мл по данным литературы колеблется от 20 до 55%.(Armitage et аl., 1988; Lange et аl., 1986; Hudson et аl., 1989). Другие авторы утверждают, что высокие значения ПСА при доброкачественных новообразованиях предстательной железы не так уж и редки.
Однако наибольшее значение определения ПСА безусловно имеет для диагностики рака предстательной железы. Следует отметить, что из трех основных исследований: определения ПСА, ректального и ультразвукового исследования предстательной железы — определение простато-специфического антигена имеет наименьшее количество ложноoтрицательных результатов и наибольшую специфичность. Серийный скрининг с применением ПСА в 2 раза увеличивает долю диагностики рака простаты в стадии Т1-Т2, в то время как пальцевое ректальное исследование выявляет лишь 30% гистологически подтвержденного рака той же стадии. До 90% рака простаты, выявляемого с помощью определения ПСА, приходится на поздние стадии заболевания. Чувствительность метода недостаточна для определения латентного, фокального, высокодифференцированного рака простаты. Так, Oesterling J. (1993) установил, что 20-40% всех злокачественных новообразований предстательной железы сопровождаются нормальной концентрацией ПСА в сыворотке крови. В то же время этот показатель при Т3-Т4 стадиях заболевания бывает положительным почти в 100% случаев.
При сравнении предоперационных уровней ПСА с результатами, полученными после простатэктомии, многие авторы отмечают высокую чувствительность и четкую корреляцию со стадией заболевания. Так из ряда работ (Stamey et аl., 1987, 1989), создается впечатление, что концентрация ПСА в сыворотке нелеченных больных пропорциональна объему опухоли в ткани простаты. Несмотря на определенную вариабильность предоперационных уровней ПСА у больных с клиническими стадиями А и В, показано, что его уровни ниже 15 нг/мл и выше 40 нг/мл являются достаточно четкими признаками отсутствия или наличия пенетрации капсулы, инвазии в семенные пузырьки и метастазов в тазовые лимфоузлы, хотя и при уровнях ПСА 15 нг/мл иногда возможна инвазия в капсулу железы.
Увеличение уровня ПСА до больших значений (около 20 нг/мл и выше) является высокоспецифичным даже при нормальных показателях ректального пальцевого исследования простаты. Поэтому при высоких цифрах ПСА биопсия предстательной железы должна проводится обязательно. Уровень ПСА более 50 нг/мл указывает на экстракапсулярную инвазию в 80% случаев и поражение регионарных лимфатических узлов у 66% больных (Stanley et аl., 1990). Исследования Rana et аl. (1992) показали, что результаты ПСА более 100 нг/мл указывают на 100% метастазирование (регионарное или отдаленное).
Наибольшие трудности возникают при интерпретации значений ПСА в диапазоне от 4 нг/мл до 20 нг/мл. Проведенные исследования свидетельствуют о том, что частота рака простаты у пациентов с концентрацией общего ПСА от 4 до 15 нг/мл и нормальными данными при пальцевом ректальном исследовании простаты достигает по разным данным от 27 до 37%.
Основным для клиницистов является осознание возможности выявления с помощью ПСА субклинических форм рака простаты без признаков экстра-капсулярной инвазии (стадии Т1 и Т2), когда возможно выполнение радикальной простатэктомии. По данным Myrtle et аl. (1986) показатели ПСА в сыворотке более 4 нг/мл наблюдались у 63% больных раком простаты стадии Т1 и у 71% — стадии Т2. В то же время, при экстракапсулярных поражениях (стадии Т3 и Т4) повышение ПСА наблюдалось в 88% случаев. В данной ситуации с целью более точной интерпретации повышенных значений общего ПСА весьма желательно исследование концентрации свободного ПСА и расчет соотношения «свободный ПСА/общий ПСА».
Помимо первичной диагностики рака простаты, определение ПСА широко применятся в следующих случаях:
1. После радикальной простатэктомии через несколько недель ПСА перестает определяться. Регулярные контрольные исследования (каждые 3 месяца) позволяют своевременно выявить рецидив заболевания в случае повышения ПСА. Если же показатели ПСА нормальны и нет клинических симптомов болезни, то исключаются другие исследования.
2. У больных, получавших лучевую терапию, отмечается значительное снижение уровня ПСА в сыворотке крови, что свидетельствует об эффективном лечении. В то же время, повышение ПСА говорит о малой чувствительности опухоли к проводимому лечению, либо о рецидиве заболевания. Следует отметить, что снижение ПСА до нормальных цифр коррелирует с уровнем антигена до лечения. Пациенты с показателями ПСА до лечения неболее 20 нг/мл имели нормальные показатели ПСА после лечения в 82% случаев. В то же время, у больных с более высокими цифрами ПСА до лечения этот процент составлял лишь 30%. Большинство пациентов со стабильным снижением ПСА оставались в ремиссии в течение последующих 3-5 лет.
3. Целесообразно определять ПСА у больных, получающих терапию антиандрогенами. Повышение уровня ПСА говорит о прогрессировании заболевания и о необходимости сменить характер лечения.
При антиандрогенном лечении уровень ПСА в сыворотке крови является точным индикатором успеха или неуспеха терапии. После начала терапии уровень ПСА быстро снижается у 50% больных (от 85 до 2.1 нг/мл), в то время как в отсутствие ответа величина ПСА не изменяется (Hudson et аl., 1989). Прогрессирование болезни наблюдалось в 50% случаев, когда уровень ПСА не снижался ниже 10 нг/мл. Это означает, что уровень ПСА не играет прогностического значения до начала терапии, в то время как в процессе лечения ПСА является хорошим индикатором эффективности терапии и хорошо коррелируется, как с выживаемостью, так и с длительностью ремиссии. Согласно Stainey (1989), повышение уровня ПСА через 6 месяцев после начала терапии может служить в качестве оценки чувствительности к проводимой терапии.
Ультразвуковая диагностика рака предстательной железы. Ультразвуковое исследование нашло очень широкое применение в диагностике многих заболеваний предстательной железы, в том числе и рака. Особенно интерес к исследованию проявился с введением трансректальной ультразвуковой томографии. Современные трансректальные ультразвуковые датчики обеспечивают очень высокое качество изображения и позволяют детально визуализировать структуру простаты, окружающих ее органов и тканей, а также прицельно взять биопсию из измененного участка железы. В норме неизмененная предстательная железа при ультразвуковом исследовании имеет треугольную форму. Основание железы обращено к прямой кишке, а верхушка — к шейке мочевого пузыря. Наибольший размер железы в поперечном направлении составляет 40-45 мм, в передне-заднем направлений он равен 20-27 мм, в продольном — 35-45 мм. На ультразвуковых томограммах различаются центральная и периферическая зоны простаты, которые обычно занимают большую часть предстательной железы. При ультразвуковом исследовании периферическая зона имеет однородную структуру и характеризуется отражениями средней интенсивности. Центральная зона расположена вокруг простатического отдела уретры, имеет ячеистую структуру, а по эхогенности ниже периферической зоны. При осмотре области шейки мочевого пузыря выделяется гипоэхогенная фибро-маскулярная строма, не содержащая желез, которая формирует переднюю часть простаты. Как считает В.Н. Шолохов (1997), с возрастом при развитии доброкачественной гиперплазии или при воспалительных заболеваниях центральная и периферическая зоны железы могут не дифференцироваться. Простатический отдел уретры выглядит в виде гипоэхогенного тяжа, проходящего в черную центральную зону железы.
Простата окружена перипростатической жировой клетчаткой и фасцией, которые формируют гиперэхогенный пограничный слой, который часто описывается как капсула железы. Истинная капсула простаты, если ее удается визуализировать, определяется в виде очень тонкой гипоэхогенной прерывистой линии по поверхности железы.
Семенные пузырьки визуализируются в виде симметричных гипоэхогенных тяжей, расположенных между простатой и мочевым пузырем размерами 2 х 7 см.
Как уже отмечалось выше, рак чаще всего развивается в периферической зоне простаты. Учитывая эту особенность, проще проводить дифференциальную диагностику с другими заболеваниями. Выявляемые структурные изменения, локализирующиеся в пределах центральной зоны, с большей вероятностью могут быть отнесены к проявлению доброкачественного процесса, в то время как обнаружение структурной перестройки, локализующейся в периферической зоне, чаще соответствует злокачественной опухоли.
Периферическая зона занимает 75% объема простаты, и в этой части железы рак возникает в 80% случаев. Большей частью опухоль располагается на глубине 3-4 мм от пограничною слоя. Центральная зона занимает около 20% объема железы. В этой части простаты развивается только 5% злокачественных новообразований. Вокруг простатического отдела уретры располагается тонкий участок железистой ткани — так называемая переходная зона. В норме она практически не дифференцируется от центральной зоны и занимает всего 5% объема простаты. В переходной зоне рак развивается в 20% случаев (Шолохов В.Н., 1997).
Наиболее характерными признаками рака простаты, локализующегося в периферической зоне, является наличие одного или нескольких узлов неправильной формы и пониженной эхогенности (рис. 4).
Рис. 4. Трансректальное исследование предстательной железы (продольная плоскость на границе периферической и переходной зоны), опухолевый узел (указан стрелкой) не выходящий за пределы органа. Признаков пенетрации капсулы нет.
Диагноз: рак предстательной железы.
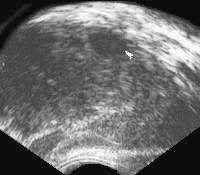
Нередко узел окружен гиперэхогенным ободком, что объясняется фиброзной реакцией соединительной ткани предстательной железы, окружающей опухолевый очаг. По мере роста опухоли появляются бугристые контуры железы с признаками пенетрации пограничного слоя (рис. 5 и рис. 6).
Рис. 5. Рак предстательной железы. Опухолевый узел в периферической зоне левой доли, инфильтрирует заднебоковую поверхность железы и перипростатической клетчатки.
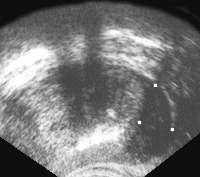
Рис. 6. Трансректальное исследование предстательной железы (поперечная плоскость). Опухолевый узел в периферической зоне левой доли. Отмечается деформация наружного контура железы, признаки пенетрации собственной капсулы. (Т3) Диагноз: рак предстательной железы.
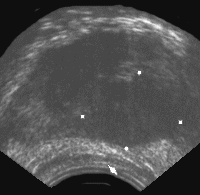
Особенно большое значение имеет выявление инфильтрации по передне-боковой поверхности железы, которая недоступна пальцевому исследованию.
Наиболее сложными для диагностики являются опухоли, которые локализуются в центральной и переходной зонах железы. Зачастую, развиваясь на фоне доброкачественной гиперплазии, рак по эхогенности практически не отличается от окружающих тканей, в связи с чем нередко возникают диагностические ошибки, а диагноз устанавливается при гистологическом исследовании удаленного материала во время операции.
По мере увеличения опухолевой инфильтрации стромы железы меняется ее ультразвуковая структура. Ткань железы становится неоднородной, с беспорядочными отражениями низкой интенсивности. Ультразвуковая томография позволяет выявить инфильтрацию капсулы простаты, семенных пузырьков мочевого пузыря, стенки прямой кишки, лимфатических узлов, что, естественно, позволяет уточнить стадию заболевания.
В отличие от рака, гиперплазия предстательной железы обычно развивается в переходной зоне по направлению к внутренней части железы. При этом переходная зона начинает сдавливать центральную и периферическую зону, вызывая их постепенную атрофию. Из центральной и периферической зон и фибромышечных слоев формируется «хирургическая капсула», по которой происходит «вылущивание» гиперплазированных узлов при операции. По мере роста доброкачественной гиперплазии железа приобретает шаровидную форму; при преимущественном росте периуретральных желез отмечается выбухание контура железы в просвет мочевого пузыря и формируется средняя доля, которая растет, оттесняя кпереди и деформируя заднюю стенку мочевого пузыря, сдавливая в значительной степени простатическую уретру и шейку мочевого пузыря. Поскольку доброкачественная гиперплазия предстательной железы не характеризуется инфильтративным ростом, то капсула железы обычно четко прослеживается по периферии среза. Частыми находками при доброкачественной гиперплазии являются мелкие ретенционные кисты и кальцинаты, генез которых связан со сдавлением протоков железы гиперплазированной тканью; располагаются они чаще всего по т.н. хирургической капсуле. При ультразвуковом исследовании простаты порой возникает необходимость проводить дифференциальную диагностику с простатитом. Это вызвано тем, что пальпация предстательной железы при простатите иногда дает результаты, очень похожие на рак. Ультразвуковое исследование в стадии отека и инфильтрации железы выявляет: увеличение железы (рис. 7 и рис. 8), изменение ее формы (чаще шаровидная) и структуры. Снижается эхогенность железы, теряется эхографическая дифференциация железистых и фибромышечных зон.
Рис. 7. Трансректальное исследование предстательной железы (поперечная плоскость). Хронический простатит с участками кальцификации в железе.
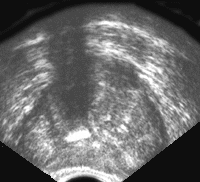
Рис. 8. Хронический простатит; усиление кровотока в ткани железы (режим энергетического Доплера).
При абсцедировании простатита — на фоне гипоэхогенной отечной ткани железы появляются анэхогенные зоны, соответствующие зонам некротических изменений. Постепенно происходит формирование стенки абсцесса в виде кистозной структуры с толстой стенкой и жидкостным неоднородным содержимым . При хроническом простатите эхоструктура железы может быть практически не изменена, либо выявляются диффузные повышенной эхогенности структуры в результате клеточной инфильтрации и склеротических изменений. Определяются кальцинаты и мелкие ретенционные кисты.
Описанные три основных метода диагностики в дальнейшем требуют обязательного морфологического подтверждения заболевания. С этой целью выполняется пункционная биопсия, которая наиболее достоверна при выполнении ее под контролем ультразвука. Особенно это касается обследования больных с малыми образованиями.
Биопсию предстательной железы можно производить через промежность, трансректально или трансуретральным доступом. Открытая биопсия применяется крайне редко. Трансуретральная резекция предстательной железы не только позволяет уточнить диагноз, но и обеспечивает восстановление мочеиспускания.
Трансвезикальная биопсия предстательной железы — вынужденная манипуляция у больных с подозреваемым раком предстательной железы, у которых в связи с острой задержкой мочеиспускания, обострением хронического пиелонефрита и высокой азотемией возникает срочная необходимость в проведении цистостомии.
В диагностике рака предстательной железы частота ложноотрицательных результатов гистологического анализа кусочков ткани при промежностном и трансректальном доступе не превышает 20%.
Осложнения пункционной биопсии встречаются крайне редко и могут быть связаны с повреждением мочевого пузыря и мочеиспускательного канала. Возможна гематурия, гематоспермия, промежностная и позадилобковая гематома. Для профилактики инфекционных осложнений, которые составляют около 2%, за сутки до биопсии и после нее назначают антибиотики.
В некоторых сложных случаях дифференциальной диагностики с успехом применяют цитологическую диагностику рака предстательной железы. Для цитологического исследования используют аспират из предстательной железы.
Цистоскопия является вспомогательным методом диагностики. При проведении цистоскопа может отмечаться девиация мочеиспускательного канала опухолевыми узлами. При цистоскопии удается обнаружить асимметричную деформацию шейки мочевого пузыря. В месте прорастания опухолью предстательной железы стенки мочевого пузыря определяется разрыхленность слизистой оболочки, фибриновые налеты, язвы или опухолевые разрастания, при этом трудно решить — прорастает ли опухоль из предстательной железы в мочевой пузырь или опухоль пузыря в железу.
Из методов диагностики рака предстательной железы заслуживает внимания рентгеновская компьютерная и магнитно-резонансная томография. Получаемая при этом информация соответствует таковой при ультразвуковом исследовании. На томограммах также видны структура предстательной железы, опухолевые узлы, их величина, степень прорастания капсулы, инфильтрация мочевого пузыря, семенных пузырьков, окружающей клетчатки. Эти методы, однако, оказались не более точными, чем трансректальное УЗИ при определении стадии ограниченного местного роста рака предстательной железы, и, более того, есть данные, что трансректальное ультразвуковое исследование дает более надежные результаты при оценке стадии заболевания.
Экскреторная урография позволяет оценить функцию почек и уродинамику верхних мочевых путей. Уретероэктазия и уретерогидронефроз являются следствием сдавления тазовых отделов мочеточников опухолью. Такие изменения часто бывают односторонними. При полной обструкции мочеточника происходит выключение почки, при этом тень рентгеноконтрастного вещества на стороне сдавления отсутствует.
Определение стадии заболевания. За установлением диагноза рака предстательной железы одновременно встает вопрос об установлении стадии заболевания, что в конце концов определяет характер будущего лечения. Кратко остановимся на возможностях применяемых методов исследования в установлении стадии заболевания.
Пальцевое исследование прямой кишки. Точность диагностики рака предстательной железы при пальцевом исследовании прямой кишки составляет 30-50%. Часто наблюдается недооценка стадии, поскольку небольшие, расположенные в передних отделах железы опухоли, как правило, не пальпируются; ложноположительные результаты наблюдаются у больных с гиперплазией предстательной железы и простатитом. Этот метод однако позволяет выявить рак предстательной железы, когда уровни ПСА остаются в пределах нормы, и предоставляют хотя не точные, но полезные данные о стадии заболевания. Пальпируемый неподвижный опухолевый инфильтрат или прорастание в кишку говорят о далеко зашедшем опухолевом процессе (Т4).
Определение простатического специфического антигена. При оценке отмечается достаточно четкая корреляция между уровнями ПСА и гистологической (и в меньшей степени клинической) стадией рака предстательной железы. У каждого конкретного больного корреляция не столь сильна из-за значительного перекрывания пределов различных возрастных норм. Уровни 10-20 нг/мл часто являются показателем опухоли, прорастающей за пределы капсулы предстательной железы, уровни выше 40 нг/мл свидетельствуют о наличии метастазов.
Хотя сывороточные уровни ПСА сами по себе не являются надежным показателем стадии заболевания, их можно использовать, чтобы избежать некоторых исследований. Выдвинуто предположение, что больным с вновь выявленным раком предстательной железы без симптомов поражения костей и при уровнях ПСА не выше 10 нг/мл не требуется проводить сцинтиграфию костей для определения стадии. У таких больных вероятность метастазов в костях приближается к нулю, хотя многие практические врачи считают этот метод исследования основным, так как при его помощи можно диагностировать «горячие точки», как например, остеоартроз позвоночника, который позже может создать путаницу в оценке симптомов. По данным Walsh et Partin (1994) при предоперационном ПСА 20нг/мл рецидива не было только у 45%.
Казалось бы приведенные цифры убедительно показывают значимость ПСА для прогноза заболевания, но тем не менее надо принимать во внимание и другие исследования. По данным Элиса (1994) у 21% больных с ПСА 3 ;
3) у 26% больных с дооперационным стадированием Т1б выявлена пенетрация капсулы, у 10% — инвазия семенных пузырьков;
4) у 37% больных с дооперационной стадией T1c найден распространенный рак (пенетрация капсулы), или опухоль по краю резекции, или инвазия семенных пузырьков, или наличие метастазов в регионарные лимфатические узлы).
Таблица 15. Ошибки клинического стадирования 3170 больных, подвергнутых радикальной простатэктомии по поводу клинически локализованного РПЖ (стадии Т2с и меньше) (Zincke et аl., 1994).
Современные методы диагностики «мужской» онкологии, или как определить рак простаты

Онкологии подвержены даже молодые люди.
О том, как должна проводиться диагностика рака простаты у мужчин разных возрастных групп, расскажем далее.
По каким симптомам можно определить онкологию?
Выявить заболевание на первой стадии можно лишь одним способом — сдав анализ под названием ПСА. Происходит это, как правило, случайно, в рамках диагностики прочих мужских проблем. Симптоматику самого рака можно легко спутать с признаками других заболеваний, например, таких, как простатит.
Если внимательно относиться к своему здоровью, то обнаружить опухоль можно уже на второй стадии, но, к сожалению, в большинстве случаев мужчины приходят к врачу на третьей-четвертой стадии, когда добиться полного выздоровления крайне сложно.
Что должно насторожить:

- учащенное мочеиспускание, как ночью, так и в дневное время;
- боли в области малого таза и/или промежности;
- болезненность и жжение при мочеиспускании;
- проблемы с потенцией, уменьшение объема спермы;
- недержание мочи;
- прерывистая или слабая струя мочи (жидкость может вытекать буквально по каплям);
- частые позывы к походу в туалет, либо ощущение, что орган опорожнен не полностью даже после факта мочеиспускания;
- боли в поясничной области.
Ранняя диагностика рака предстательной железы у мужчин
 В возрасте до 50 лет проблема встречается достаточно редко: лишь 2-3 представителя мужской половины человечества из 1000 сталкиваются с диагнозом «онкология».
В возрасте до 50 лет проблема встречается достаточно редко: лишь 2-3 представителя мужской половины человечества из 1000 сталкиваются с диагнозом «онкология».
Среди мужчин за 60 статистика уже совсем другая: болеет один из ста. При приближении к восьмидесятилетнему возрасту риск возрастает еще в десятки раз: рак поражает каждого восьмого мужчину.
Вывод один: находящимся в группе риска стоит внимательно следить за собственным здоровьем, а также периодически сдавать анализы.
Раннее диагностирование включает:
- экспресс-тест на выявление простат-специфического антигена в крови. Исследование называют сокращенно: ПСА;
- анализ крови и мочи;
- внешнее пальпационное обследование, которое проводит уролог.
Наблюдательная тактика
В 90% случаев мужскую онкологию лечат при помощи лучевой терапии, остальные 10% приходятся именно на тактику активного наблюдения.
Наблюдательная тактика имеет не только множество сторонников, но и противников.
Медицинское сообщество делится на два лагеря: одни убеждены, что те, у кого риск смерти от рака простаты низкий, могут жить достаточно долго (до 10 лет) и без применения агрессивных методов лечения, другая же часть врачей-урологов считает, что такая тактика приводит к росту смертности.
Трансректальная пальцевая проверка
Несмотря на существование других методик исследования состояния предстательной железы, пальпационный метод остается достаточно популярным. Многое зависит от квалификации доктора, а также того, насколько точно пациент может описать испытываемые ощущения.
 Что удается выявить:
Что удается выявить:
- степень разрастания железы;
- присутствие плотных узлов;
- наличие уплотнений с четкими границами.
Основные недостатки метода: эффективность сильно зависит от квалификации врача, на 1-2 стадии выявить рак таким способом практически невозможно, дискомфорт, испытываемый пациентом (указательный палец вводится в анальное отверстие на 3-5 см, затем начинается пальпационный осмотр).
 Под скринингом понимается комплексное диагностическое мероприятие, включающее регулярное измерение показателя ПСА в крови с последующей систематической биопсией при обнаружении повышенного показателя (более 4 нг/мл).
Под скринингом понимается комплексное диагностическое мероприятие, включающее регулярное измерение показателя ПСА в крови с последующей систематической биопсией при обнаружении повышенного показателя (более 4 нг/мл).
Показания для проведения скрининга:
- возраст от 40 до 50, если хотя бы у одного из родственников мужчины диагностирован рак предстательной железы;
- возраст от 50 до 70 лет — для всех остальных категорий.
УЗИ простаты
 Ультразвуковое исследование простаты может проводиться несколькими способами: трансректально (через прямую кишку), трансуретрально (датчик вводится в мочеиспускательный канал), а также наружным способом (через промежность или брюшную стенку).
Ультразвуковое исследование простаты может проводиться несколькими способами: трансректально (через прямую кишку), трансуретрально (датчик вводится в мочеиспускательный канал), а также наружным способом (через промежность или брюшную стенку).
Врач оценивает форму и объем железы, ее структуру, а также прочие важные показатели.
Внешний способ осмотра существенно уступает трансректальному. Эффективность последнего достигает примерно 80%. Трансуретральная методика достаточно сложна, требует применения анестезии и высокой квалификации доктора, проводящего обследование.
Уретроскопия и цистоскопия
 При уретроскопии мочеточник исследуют с помощью специального инструмента — уретроскопа. Он вводится непосредственно в орган. Метод применяется, как правило, для исследования уретры, а также почечных лоханок.
При уретроскопии мочеточник исследуют с помощью специального инструмента — уретроскопа. Он вводится непосредственно в орган. Метод применяется, как правило, для исследования уретры, а также почечных лоханок.
Цистоскопия — исследование мочевого пузыря с помощью специального инструмента цистоскопа, вводимого в мочевой пузырь через канал мочеиспускания.
Оба способа при диагностике онкологических заболеваний предстательной железы используются лишь косвенно, например, если у мужчины есть жалобы, а признаки рака при углубленном исследовании не выявляются.
Тест на простатический специфический антиген в крови (ПСА)
Указанный антиген является белком, который вырабатывается исключительно в предстательной железе. Выброс в кровь в больших количествах является тревожным сигналом.
Нормы показателя следующие (лучше, если значение стремится к нулю):

- до 50 лет ПСА не должен превышать 2,5 нг/мл;
- если возраст мужчины от 50 до 60 лет, то норма антигена повышается до 3,5 нг/мл;
- от 0 до 4,5 нг/мл — допустимый диапазон для возрастной группы от 60 до 70 лет;
- для мужчин более старшего возраста допустимым считается значение до 6,5 нг/мл.
Основное преимущество указанного теста состоит в том, что он позволяет быстро и легко поставить точный диагноз и уточнить, страдает ли мужчина именно от онкологии, или причиной нарушений в состоянии здоровья являются иные заболевания предстательной железы и/или мочеполовой системы.
Относительно недавно появился молекулярный ПСА тест, который является самым современным способом верифицировать рак предстательной железы. Благодаря этому тесту частота проводимой у пациентов биопсии сократилась сразу на треть.
Как еще можно диагностировать онкозаболевание?
 Основные методы диагностики были перечислены выше.
Основные методы диагностики были перечислены выше.
Иногда в дополнение к ним назначается КТ или МРТ, но их проводят в том случае, если онкология уже диагностирована, и есть необходимость определить размер опухоли, ее структуру и прочее.
Отдельно стоит сказать об анализе мочи, который имеет достаточно высокую информативность. Определяют обычно три составляющих: наличие лейкоцитов, анализ онкомаркера UBS, уровень гемоглобина.
Гистология
Биопсию предстательной железы проводят через прямую кишку.
С помощью УЗИ-зонда врач контролирует процесс «операции», а специальный аппарат, называемый пистолетом, производит забор тканей с разных участков предстательной железы.
Как правило, требуется не менее 10-12 точек забора. Метод достаточно эффективен, однако может быть ошибочным, если опухоль слишком мала, находится в труднодоступном месте, либо обследование проводилось с использованием старого способа (не пистолета, а иглы для забора).
Морфологическая верификация онкологического заболевания
 Под морфологической диагностикой понимается определение гистогенеза тканей опухоли.
Под морфологической диагностикой понимается определение гистогенеза тканей опухоли.
При определении рака предстательной железы основным способом верификации является проводимое гистологическое обследование — биопсия.
Забор тканей позволяет определить степень поражения клеток, тканей, степень разрастания новообразования и прочее.
Видео по теме
О методах диагностика рака предстательной железы у мужчин в видео:
Несмотря на трудности в выявлении рака предстательной железы, с каждым годом врачам удается добиться определенного прогресса. Благодаря ранней и своевременной диагностике мужчины обретают шанс на долгую и полноценную жизнь.
Методы диагностики рака предстательной железы
 Диагностика рака предстательной железы позволяет выявить наличие нарушений структуры органа, фиксировать появление злокачественных образований, изменение их размеров и формы с целью своевременного проведения терапии. Онкологические образования в различных частях простаты на первых этапах после инфицирования вирусом впч практически не имеют симптомов, что затрудняет проведение диагностики на предмет патологий в органе. Результаты онкологии в области простаты находятся на втором месте по частоте возникновения, уступая лишь количеству злокачественных структур в органах дыхания человека. Более 50% мужчин в возрасте 40 – 50 лет имеют те или иные формы образований в структуре. После явного проявления симптомов, болезнь характеризуется динамичным развитием и в течение нескольких лет может привести к летальному исходу.
Диагностика рака предстательной железы позволяет выявить наличие нарушений структуры органа, фиксировать появление злокачественных образований, изменение их размеров и формы с целью своевременного проведения терапии. Онкологические образования в различных частях простаты на первых этапах после инфицирования вирусом впч практически не имеют симптомов, что затрудняет проведение диагностики на предмет патологий в органе. Результаты онкологии в области простаты находятся на втором месте по частоте возникновения, уступая лишь количеству злокачественных структур в органах дыхания человека. Более 50% мужчин в возрасте 40 – 50 лет имеют те или иные формы образований в структуре. После явного проявления симптомов, болезнь характеризуется динамичным развитием и в течение нескольких лет может привести к летальному исходу.
Различные способы диагностики позволяют обнаружить рак простаты до выхода процесса в необратимую стадию. Существующие методики обнаружения злокачественных образований, различаются между собой по:
- степени болезненности при проведении;
- достоверности получаемых данных;
- возможности диагностики ранних стадий развития онкологических структур;
- необходимости проникновения в организм диагностических устройств или ее отсутствием.
В большинстве случаев после осмотра уролога и назначения первичной диагностики, по ее результатам и при необходимости детализации нарушения применяются более дорогостоящие и сложные методы.
Причинами обращения к врачу при подозрении наличия диагноза рак предстательной железы у мужчин являются дисфункция процесса мочеиспускания, болевые ощущения при половом акте. Существует ряд симптомов, при наличии которых у пациента врач может заподозрить наличие онкологии. К наиболее распространенным проявлениям нарушений относят:
 Болевые ощущения, которые на первом этапе развития опухоли приводят к передавливанию каналов для выведения мочи в области простаты. Характерными особенностями нарушений на этой стадии являются: чувство неполного опорожнения, трудности при начале мочеиспускания, выход мочи в виде тонкой струйки с характерными паузами и специфичным нехарактерным запахом, учащение позывов к опустошению мочевого пузыря, недержание.
Болевые ощущения, которые на первом этапе развития опухоли приводят к передавливанию каналов для выведения мочи в области простаты. Характерными особенностями нарушений на этой стадии являются: чувство неполного опорожнения, трудности при начале мочеиспускания, выход мочи в виде тонкой струйки с характерными паузами и специфичным нехарактерным запахом, учащение позывов к опустошению мочевого пузыря, недержание.- На втором этапе происходит расширение области локализации опухоли, при котором она выходит за границы простаты. Проявлениями симптомов болезни на этой стадии является: болевые ощущения в области промежности и лобка, недержание, боли в области поясницы, отдающие в мошонку и область желчного пузыря, нарушение эрекции, кровяные выделения в семенной жидкости и моче.
- На последнем этапе происходит поражение соседних структур вирусом впч в ходе вторичного инфицирования. Эта стадия проявляется в виде болевых ощущений в костях, ограничении работы опорно-двигательного аппарата, с возможностью наступления паралича, отеки в области нижних конечностей, беспричинная и стремительная потеря массы тела, снижение работоспособности и ухудшение аппетита.
Прием у врача
При наличии перечисленных симптомов, больной обращается за помощью к специалисту, который проводит его осмотр и назначает проведение диагностических процедур.
Постановкой диагноза, назначением анализов и их расшифровкой занимается квалифицированный уролог-онколог.
Первичная диагностика включает:
- сбор данных анамнеза;
- опрос пациента и фиксация симптомов болезни;
- оценка общего состояния, измерение массы тела, кожных покровов, лимфатической системы и печени.
 С целью предупреждения рака простаты проведение экспресс-методик, осмотра и скрининг-тестов рекомендуется выполнять ежегодно всем мужчинам в возрасте свыше 40 лет, даже без клинических проявлений болезни. Современные методы диагностики позволяют определить наличие онкологического заболевания на стадии зарождения при отсутствии проявленной симптоматики новообразования. Результаты обследования предоставляются пациенту в течение от 3 – 4 ч до нескольких дней.
С целью предупреждения рака простаты проведение экспресс-методик, осмотра и скрининг-тестов рекомендуется выполнять ежегодно всем мужчинам в возрасте свыше 40 лет, даже без клинических проявлений болезни. Современные методы диагностики позволяют определить наличие онкологического заболевания на стадии зарождения при отсутствии проявленной симптоматики новообразования. Результаты обследования предоставляются пациенту в течение от 3 – 4 ч до нескольких дней.
Методы диагностики онкологии в предстательной железе
В зависимости от проявления признаков болезни и ее симптоматики, врач может назначить проведение первичных методов обследования, к которым относятся:
- пальцево-ректальный анализ;
- взятие клинического и биохимического анализов мочи и крови;
- экспресс-тест, определяющий уровень простато-специфического антигена (ПСА).
При получении сомнительных данных или подозрении на наличие онкологических образований в простате, выявленных в ходе проведения первичной диагностики, врач назначает одну из методик вторичного ряда:
 УЗИ, ТРУЗИ, ТУУЗИ;
УЗИ, ТРУЗИ, ТУУЗИ;- биопсию;
- цистоскопию или уретроскопию;
- рентгенографическое исследование простаты;
- радиоизотопное сканирование;
- магнитно-резонансную томографию с использованием контрастного вещества.
Ниже описаны различные методики диагностики онкологических структур в предстательной железе с обозначением их особенностей, преимуществ и недостатков.
Ректальный метод исследования
Этот метод исследования наличия опухоли и ее размеров проводится в коленно-локтевой позиции, положении лежа и на правом боку.
Ректальное исследование области прямой кишки относится к безопасным и дешевым методам проверки наличия раковых образований в простате, при его помощи осуществляется ранняя диагностика рака предстательной железы.
Пальцевая трансректальная диагностика способна определить не только наличие поражения, но и его природу. Симптомами опухоли простаты являются:
- несимметричные контуры органа;
- уплотненная консистенция отдельных участков предстательной железы, наличие скоплений инфильтрата или узловых образований вплоть до поражения клеток таза;
- прощупываемые образования семенных пузырьков;
- сращивание железы с соседними структурами и потеря подвижности.
 Пальцевое обследование проводится урологом, который вводит в прямую кишку указательный палец на 3 – 5 см внутрь анального отверстия мужчины и выполняет прощупывание простаты. На чувствительность пациента и результат обследования может влиять избыточный вес больного, который способствует снижению сенсорной способности исследуемого участка. В здоровом состоянии железа имеет треугольную форму с объемом, не превышающим 30 см 3 .
Пальцевое обследование проводится урологом, который вводит в прямую кишку указательный палец на 3 – 5 см внутрь анального отверстия мужчины и выполняет прощупывание простаты. На чувствительность пациента и результат обследования может влиять избыточный вес больного, который способствует снижению сенсорной способности исследуемого участка. В здоровом состоянии железа имеет треугольную форму с объемом, не превышающим 30 см 3 .
Результаты ректального обследования прямой кишки обладают низкой степенью достоверности получаемых результатов, поскольку только у трети пациентов, имеющих нарушения, диагностируемые при проведении пальцевой пальпации, подтверждается наличие патогенных новообразований. Низкая точность данных обследований объясняется невозможностью определять небольшие опухоли, расположенные в переднем отделе железы. Присущая методу вероятность появления ложноположительных результатов увеличивается при наличии у пациента при гиперплазии простаты.
Образование инфильтрата опухолевого типа или проникновение повреждения в область кишки свидетельствуют о тяжелой стадии болезни.
Особенности пальпации
При проведении трансректального пальцевого исследования существует масса особенностей, учет которых повысит точность результата обследования:
 На первой стадии развития патология не диагностируется, на второй можно нащупать небольшие участки уплотнения тканей, множественные или единичные образования узелкового типа. Наличие узелка большого размера свидетельствует о локальном образовании структуры, содержащей вирус впч. Размеры и структура самой простаты остаются в неизменном состоянии.
На первой стадии развития патология не диагностируется, на второй можно нащупать небольшие участки уплотнения тканей, множественные или единичные образования узелкового типа. Наличие узелка большого размера свидетельствует о локальном образовании структуры, содержащей вирус впч. Размеры и структура самой простаты остаются в неизменном состоянии.- На второй стадии происходит увеличение железы, по мере развития раковых клеток происходит изменение ее консистенции на твердую или хрящевидную структуру. В редких случаях на этом этапе удается обнаружить инфильтрат, расположенный в направлении семенных пузырьков. При дальнейшем разрастании опухоли расширяется область ее локализации с повреждением окружающих тканей, границы новообразования размываются.
Ректальное пальцевое обследование может определить с известной вероятностью не только наличие злокачественных структур в органе, но и их природу и характер.
Анализ крови на ПСА
 ПСА представляет собой белковое вещество, вырабатываемое простатой, уровень этого антигена определяется при заборе и исследовании венозной крови. Изучение концентрации специфического антигена простаты используется для выявления онкогенных заболеваний на ранней стадии без явных симптомов поражения органа. Прогрессированию злокачественного образования сопутствует увеличение содержания ПСА в крови. Однако, поскольку изменение уровня белкового вещества может вызвано физическими нагрузками на простату, эякуляцией перед проведением обследования или аденомой, рекомендуется взятие нескольких проб для изучения концентрации в течение 2 – 3 дней.
ПСА представляет собой белковое вещество, вырабатываемое простатой, уровень этого антигена определяется при заборе и исследовании венозной крови. Изучение концентрации специфического антигена простаты используется для выявления онкогенных заболеваний на ранней стадии без явных симптомов поражения органа. Прогрессированию злокачественного образования сопутствует увеличение содержания ПСА в крови. Однако, поскольку изменение уровня белкового вещества может вызвано физическими нагрузками на простату, эякуляцией перед проведением обследования или аденомой, рекомендуется взятие нескольких проб для изучения концентрации в течение 2 – 3 дней.
Нормальный показатель ПСА колеблется в зависимости от возраста пациента в диапазоне 2,5 нг/мл для 50 лет до 6,5 нг/мл при общей тенденции увеличения концентрации с возрастом мужчины. Повышение содержания белкового компонента до 10 – 20 нг/мл свидетельствует об опухоли, выходящей за границы простаты, а концентрация ПСА свыше 40нг/мл говорит о развитии метастазов. Увеличение уровня антигена в организме может быть вызвано действием множества факторов, в связи с чем после предварительной постановки диагноза врач рекомендует его подтверждение проведением гистологического исследования.
Анализ мочи для определения онкологии
Это исследование направлено на фиксацию отклонения от нормы таких показателей, как:
- Содержание лейкоцитов, которые при нормальной работе органов мочевыделительной системы отсутствуют, их появление в заметном количестве указывает на наличие проблем в мочеполовой системе и с высокой долей вероятности свидетельствует о развитии злокачественных образований.
- Онкомаркера UBS, который представляет собой белковую структуру в составе мочи, появление которой достоверно свидетельствует о наличии в области простаты раковых клеток.
Анализ мочи проводится для определения наличия возбудителя инфекции, показателей кислотности и плотности, мочевой жидкости, количества токсичного вещества билирубина.
УЗИ простаты
Существует множество методов диагностики нарушений в области предстательной железы при помощи ультразвука, среди которых наиболее известными являются:
 наружное обследование, проводится через брюшную стенку;
наружное обследование, проводится через брюшную стенку;- наружный метод, проводимый через промежность;
- трансректальный метод, выполняемый через прямую кишку при помощи у/зв зонда;
- трансуретральная методика, предусматривающая введение регистрирующего устройства в область мочеиспускательного канала.
Наружное исследование с использованием ультразвука характеризуется технической простотой реализации, отсутствием неприятных ощущений для пациента и отсутствием противопоказаний для большинства мужчин. Ограничением для его выполнения может быть наличие дренажной системы или швов после проведения операции в месте обследования. Для определения рака в области предстательной железы выполняется диагностика при заполненном мочевом пузыре. Стандартная программа предусматривает проведение сканирования в поперечном и продольном направлениях, однако, при необходимости существует возможность выбора любой доступной плоскости. К недостаткам способа следует отнести низкую разрешающую способность, технически позволяющую определить лишь изменение очертаний или размеров железы.
Учитывая недостатки наружного сканирования, врач может рекомендовать использовать трансректальное ультразвуковое исследование (ТРУЗИ), обладающее точностью 4/5. При его проведении заполненный объем мочевого пузыря не относится к условиям, необходимым для проведения диагностики.
Наглядную картину состояния предстательной железы предоставляет трансуретральное ультразвуковое исследование (ТУУЗИ). Однако способ не получил широкого распространения, поскольку требует проведения местной анестезии, имеет риск повреждения уретры, учитывая проблематичность проведения регистрирующего устройства через канал уретры.
Специфика проведения УЗИ
При проведении изучения простаты с использованием ультразвука, необходимо учитывать, что центральная область органа имеет более низкую эхогенность, чем периферийные участки предстательной железы.  В области периферии, занимающей больше 70: общего объема органа, на расстоянии в несколько миллиметров от края образования злокачественные образования могут выявляться в ¾ случаев. Нарушения, выявленные в центральной части предстательной железы, в большинстве случаев соответствуют доброкачественным опухолям.
В области периферии, занимающей больше 70: общего объема органа, на расстоянии в несколько миллиметров от края образования злокачественные образования могут выявляться в ¾ случаев. Нарушения, выявленные в центральной части предстательной железы, в большинстве случаев соответствуют доброкачественным опухолям.
Признаками рака предстательной железы при обнаружении нарушения в области периферии являюется снижение эхогенности участка и присутствие на нем одной или нескольких структур узелкового типа, имеющих неправильную форму. Наличие темных участков на узи может свидетельствовать о наличии злокачественного образования. Изучение при помощи ультразвука позволяет оценить наличие патологий в простате, определить участки с измененными показателями эхогенности, которые, будут использоваться в качестве мест для взятия проб материала при проведении биопсии.
Биопсия представляет собой гистологическое изучение образцов тканей, отбираемых из области предполагаемой локализации нарушения, выполняемое по методу трансректального изучения. В современных центрах забор тканей и проведение исследования выполняется при помощи зонда УЗИ. Пациенту в область прямой кишки внедряется зонд, врач отмечает необходимые для забора ткани участки предстательной железы. Затем по специальному каналу устройства внедряется игла, вмонтированная в устройство, называемое пистолетом. По достижении цели игла выстреливает в простату, забирая частицу ее ткани. Для получения точного результата необходимое число точек составляет 12 шт.
Пробы, взятые с разных участков железы, отправляются в лабораторию для проведения их исследования на предмет наличия вируса впч. При проведении биопсии без дополнительных методов исследования на начальном этапе болезни или без использования УЗИ может показать отрицательный результат даже при наличии раковых клеток. Устройство с иглой может пройти место локализации новообразования и взять образец ткани со здорового участка. Однако в случае предварительного проведения изучения концентрации ПСА, которое до и после проведения биопсии показывают увеличенную концентрацию антигена, врач назначает повторное проведение операции.
Своевременное обнаружение онкологических образований в области предстательной железы позволяет предотвратить возникновение осложнений, и даже летальный исход.
На практике чаще всего используется комбинированная диагностика рака простаты, поскольку, учитывая недостатки и ограничения каждого из них, ни один не может с вероятностью 100% определить наличие злокачественного образования в клетках простаты.
Источники: http://medi.ru/info/11151/, http://prostata.guru/prostata/rak-prostaty/diagnostika.html, http://proprostatu.ru/diagnostika/metody-diagnostiki-raka-predstatelnoj-zhelezy.html














































